Коронавирус SARS-CoV-2 (severe acute respiratory syndrome coronavirus 2) относится к семейству Coronaviridae, подсемейству Coronavirinae, роду Betacoronavirus. Коронавирусы широко распространены среди мле-копитающих и птиц и вызывают респираторные, кишечные, неврологические заболевания, а также гепатит [1]. Подсемейство Coronavirinae включает 4 рода: Alfacoronavirus, Betacoronavirus, Gammacoronavirus и Deltakoronavirus. Заболевание, вызванное SARSCoV-2, получило название COVID-19.
Для проникновения в клетку коронавирусы используют S белок − гликопротеин, образующий вирусные шипы, который является основной мишенью для нейтрализующих антител [2]. S белок состоит из двух субъединиц: вариабельной S1, включающей ре-цептор-связывающий сайт, и более консервативной S2, ответственной за слияние вирусной и клеточной мембран. Рецептором для вирусов SARS-CoV-1 и SARS-CoV-2 служит ангиотензин-превращающий фермент 2 – ACE2 (angiotensin-converting enzyme 2), а для вируса MERS-CoV (Middle East respiratory syndrome) – дипептидилпептидаза-4 DPP4 (dipeptidyl peptidase 4) [3]. Показано, что SARS-CoV-2 обладает в 10-20 раз более высокой аффинностью к ACE2, чем SARS-CoV-1 [4], что обеспечивает его повышенную контагиозность.
У значительной части пациентов, зараженных SARS-CoV-2, болезнь протекает бессимптомно или вызывая слабые респираторные симптомы. Однако почти у 55% симптоматических пациентов примерно к восьмому дню заболевания появляется дыхательная недостаточность из-за развития пневмонии с двусторонней множественной долевой и субсег-ментарной зоной консолидации [5]. У 29% из этих пациентов пневмония переходит в тяжелую стадию с развитием цитокинового шторма и острого респираторного дистресс-синдрома (ОРДС), часто приводящего к смертельному исходу [5-7].
Подобно SARS-CoV-1 и MERS-CoV [8, 9], инфекция SARS-CoV-2 вызывает повышенную секрецию провоспалительных цитокинов и хемокинов, таких как IL1β (interleukin 1β), IFNγ (interferon γ), IP10 (IFN inducible protein 10), MCP1 (monocyte chemoattractant protein 1), IL4 и IL10, а у пациентов с более тяжелым течением заболевания, нуждающихся в интенсивной терапии, в плазме крови наблюдаются высокие уровни IL2, IL7, IL10, GMCSF (granulocyte-macrophage colony-stimulating factor), IP10, MCP1, MIP1α (macrophage inflammatory protein α) и TNFα (tumor necrosis factor α), свидетельствующие о цитокиновом шторме [5, 10]. Патологоанатомическое обследование умерших пациентов показало, что легкие являются основным поврежденным органом, а присутствие SARS-CoV-2 наблюдалось не только в альвеолярных эпителиальных клетках, но и в альвеолярных макрофагах, в макрофагах в лимфатических узлах и в селезенке [11].
Во время вспышки SARS-CoV-1 в 2003 г. у больных была зафиксирована связь между тяжестью заболевания и ранним развитием антительного ответа. Было замечено, что у пациентов с тяжелым течением заболевания, которым требовался дополнительный кис-лород и госпитализация в отделение интенсивной терапии (ОИТ), первые антитела появлялись уже на 4-й день заболевания, отмечалась ранняя сероконверсия антител (<16 дней), сопровождающаяся высокими титрами IgG [12, 13]. У таких пациентов болезнь чаще заканчивалась летальным исходом. В более легких случаях специфичные антитела появлялись спустя 2-3 недели после инфицирования с достижением сероконверсии в среднем через 20 дней [13-15]. Титры антител у пациентов, перенесших бессимптом-ную инфекцию, были низкими, и сероконверсии встречались редко.
Аналогично у пациентов, инфицированных SARSCoV-2, тяжелое течение заболевания коррелирует с более высокими титрами антител по сравнению с пациентами с легким течением заболевания [5]. У пациентов, госпитализированных в ОИТ, раннее появление нейтрализующих антител было зафиксировано уже через 5-14 дней после появления симптомов [16].
Одной из причин раннего антительного ответа может являться наличие В-клеток памяти, образовавшихся при предшествующей инфекции антигенно-родственными патогенами. Известно, что бетакоронавирусы могут индуцировать кросс-реактивные антитела друг против друга даже при отсутствии высокой гомологии S белка. Так, при инфекции ко-ронавирусом человека OC43 индуцировались антитела против SARS-CoV-1, и наоборот [17, 18]. В сыворотках пациентов, переболевших SARS-CoV-1, были найдены нейтрализующие антитела к более позднему вирусу MERS-CoV [17, 19], а в сыворотках крови здоровых доноров в 3% случаев были обнаружены нейтрализующие антитела к SARS-CoV-2 [16].
На примере SARS-CoV-1 было показано, что антитела к S белку могут усиливать патологию инфекции за счет антитело-зависимого усиления заболевания – ADE (antibody-dependent enhancement) [20]. С использованием сывороток пациентов, переболевших SARS-CoV-1, был картирован иммунодоминантный B-клеточный эпитоп в S белке (597-603), индуцирующий антитела, которые усиливали инфекцию как in vitro, так и in vivo на модели приматов [21]. Феномен ADE известен для различных вирусных инфекций. В конце 1960-х гг. вакцинация детей против респираторно-синцитиального вируса (RSV) привела к госпитализации 80% детей с тяжелым респираторным заболеванием, при этом двое детей умерли. Предполагается, что причиной этого катастрофического результата вакцинации было развитие ADE [22, 23]. ADE также описано для вируса денге, вируса гриппа, вируса Эбола [24-27].
Механизм ADE при коронавирусной инфекции состоит в том, что анти-S IgG в организме больного связываются с поверхностным S белком вируса, образуя иммунные комплексы. Эти комплексы способны связываться с поверхностью иммунокомпетентных клеток, включая моноциты, макрофаги или B-клетки, посредством взаимодействия Fc фрагмента антител с Fcγ рецептором (FcγR), экспрессированным на поверхности этих клеток [28]. Таким образом, макрофаги могут фагоцитировать иммунные комплексы через альтернативный механизм, не связанный с рецептором АСЕ2, отсутствующим у макрофагов. Также описано, что при взаимодействии нейтрализующих анти-S IgG с рецептор-связывающим сайтом S белка SARS-CoV-1 индуцируется его конформационное изменение с последующей активацией белка слияния, делая возможным инфицирование макрофагов, приводящее к транскрипции генома [29, 30]. Хотя инфицирование макрофагов коронавирусами не приводит к продуктивной инфекции, их взаимодействие с вирусом вызывает поляризацию функционального состояния в сторону провоспалительных макрофагов M1 (Рис. 1).
Накопление макрофагов M1 в легких приводит к повышенной продукции хемокинов, таких как MCP1(CCL2) и IL8(CXCL8), вызывающих инфильтрацию легких провоспалительными лейкоцитами. В результате этого в легочной ткани происходит резкое нарастание воспаления, сопровождаемого гиперцитокинемией и развитием ОРДС [31, 32]. Показано, что развитие процесса зависит от концентрации и аффинности анти-S IgG. ADE наступало при субоптимальной концентрации антител или их низкой аффинности, недостаточной для нейтрализации вируса [33, 34]. В модельном эксперименте на макаках было показано, что нейтрализующие анти-S IgG снижали титр вируса у животных, но одновременно значительно усиливали легочную патологию [31]. Снижение патологии достигалось блокадой FcγR макрофагов [31]. Таким образом, иммунные комплексы играли ключевую роль в развитии ADE, а наблюдаемые повреждения органов при тяжелой инфекции были вызваны не избыточным размножением вируса, а гиперактивацией врожденного воспалительного ответа [14]. Можно предположить, что механизм ADE лежит в основе осложненного течения заболевания COVID-19, наблюдаемого при раннем развитии антительного ответа, обусловленного наличием В-клеток памяти – потенциальных продуцентов антител к S белку родственных коронавирусов.
Исследования по выявлению естественного хозяина SARS-CoV-1 в Китае показали, что близкородственный вирус циркулирует в подковоносых летучих мышах, относящихся к роду Rhinolophus, семейству Rhinolophidae, отряду Chiroptera [35, 36]. Сиквенс первых штаммов SARS-CoV-2 имеет до 86.9% гомологии с ранее выделенным в Китае коронавирусом летучих мышей bat-SL-CoVZC45 [37]. Гомология S белка SARSCoV-2 с другими коронавирусами летучих мышей составляет от 75.7% до 97.7% [38, 39]. Следовательно, у людей, контактирующих с летучими мышами, могут быть антитела или B-клетки памяти, распознающие SARS-CoV-2 антигены, вследствие переболевания антигенно близкими коронавирусами летучих мышей, способными вызывать легкую или бессимптомную инфекцию.
Летучие мыши используются в пищу в Южном Китае и других странах этого региона. Живых летучих мышей часто можно увидеть на рынках и в ресторанах на юге Китая, что значительно облегчает их контакт с другими животными и с людьми и может явиться причиной инфицирования людей [20]. Наличие повышенных титров антител к вирусам, близким SARS-CoV-1, у людей, связанных с рынками по продаже живых животных, подтверждает факт инфицирования людей вирусами от летучих мышей [40]. Эффект ADE может объяснить повышенное число тяжелых случаев COVID-19 со смертельным исходом в Китае среди людей, связанных с такими рынками [5].
После появления в 2002/2003 г. SARS-CoV-1, вы-звавшего эпидемию атипичной пневмонии, изучение циркуляции коронавирусов в мире выявило большое количество летучих мышей, являющихся природным резервуаром коронавирусов, не только в Китае, но и во многих странах Европы и Америки, а также в Австралии [41]. Летучие мыши являются единственным представителем млекопитающих, способных к активному полету. Необходимость летать приводит к повышенному клеточному метаболизму с повышением температуры тела до 41℃, что сопряжено с повреждениями геномной ДНК. Эволюция летучих мышей сделала возможным предотвращение воспалительных реакций путем ослабления цитоплазматических сенсоров аномальных ДНК и ДНК патогенов, таких как STING (stimulator of interferon genes), а также снижение уровня выработки воспалительных цитокинов, например TNFα [42, 43]. Вследствие снижения интенсивности защитных воспалительных реакций повысилась чувствительность клеток летучих мышей к заражению вирусами, что было компенсировано выработкой более эффективных противовирусных мер, таких как конститутивная экспрессия IFN и наличие уникальных ISG (interferon-stimulated genes). За счет мощной системы IFN ответа и идеальной регуляции воспалительных реакций летучие мыши приобрели высокую устойчивость к вирусным инфекциям [42, 43]. РНК-содержащие вирусы репродуцируются в этих животных до высоких титров и персистируют, не нанося существенного вреда их здоровью. В результате огромное множество летучих мышей потенциально является источником вирусных инфекций для животных и людей. Среди них отмечаются опасные инфекции, включая коронавирусы (SARS-CoV-1, MERS-CoV), филовирусы (вирусы Ebola и Marburg), хенипавирусы (вирусы Hendra и Nipah) [44]. Появление в 2019 г. SARS-CoV-2 инфекции является еще одним ярким примером. Люди, обладая менее совершенным механизмом контроля над воспалением, нежели летучие мыши, могут иметь патологический ответ системы врожденного иммунитета, каким является цитокиновый шторм и ОРДС.
Летучие мыши живут колониями, насчитывающими сотни особей. Гнезда животных часто расположены в парках и в непосредственной близости от жилых домов. В общественное пространство мыши выделяют вирусы с фекалиями, в которых количество вируса может достигать 2.4х108 копий/г [45]. В Европе все виды летучих мышей оберегаются и находятся под защитой Директивы Европейского Союза о сохранении естественной среды обитания и дикой фауны и флоры [46] и Соглашения о сохранении летучих мышей в Европе [47].
Из четырех известных родов коронавируса от летучих мышей выделялись только два: Alfacoronavirus и Betacoronavirus. Начиная с 2010 г., альфа-и бета-коронавирусы постоянно регистрируются в летучих мышах Италии [48-50], при этом в провинциях Пьемонт и Лигурия выявленное заражение колоний составляет до 26% [51]. В 13 регионах Испании обследование 576 особей различных видов летучих мышей позволило идентифицировать 14 новых альфа-и бетакоронавирусов [52]. В Нидерландах бетакоронавирусы были выделены из 211 летучих мышей в 31 населенном пункте. При этом основным носителем оказались летучие мыши рода Pipistrellus, широко распространенные в городских районах. Выявленная зараженность летучих мышей коронавирусами в Нидерландах составила 16.9% [53], а во Франции – 37.9% [54]. Однако распространение летучих мышей, носителей коронавирусов, неоднородно. Так, в Германии при изучении 653 летучих мышей в трех регионах коронавирусы встречались значительно реже, лишь в 1.4-3.1% случаев [55]. С гораздо большей частотой (от 25,8% до 65%) в Германии обнаруживались астровирусы (семейство Astroviridae).
Во многих европейских странах, включая Италию, Испанию, Францию и Болгарию, выделялись SARS-CoV-1-подобные бетакоронавирусы, при этом, как и в Китае, эти вирусы были выделены от подковоносых летучих мышей рода Rhinolophus [51], подтверждая специфичность данного хозяина для SARS-CoV-1-подобных вирусов. На Рис. 2 показано распространение летучих мышей рода Rhinolophus, носителей SARS-CoV-1, в мире. Важно отметить, что, помимо Китая и стран Юго-Восточной Азии, данный род летучих мышей широко представлен в странах Южной Европы и Ближнего и Среднего Востока, но отсутствует в Северной Европе.
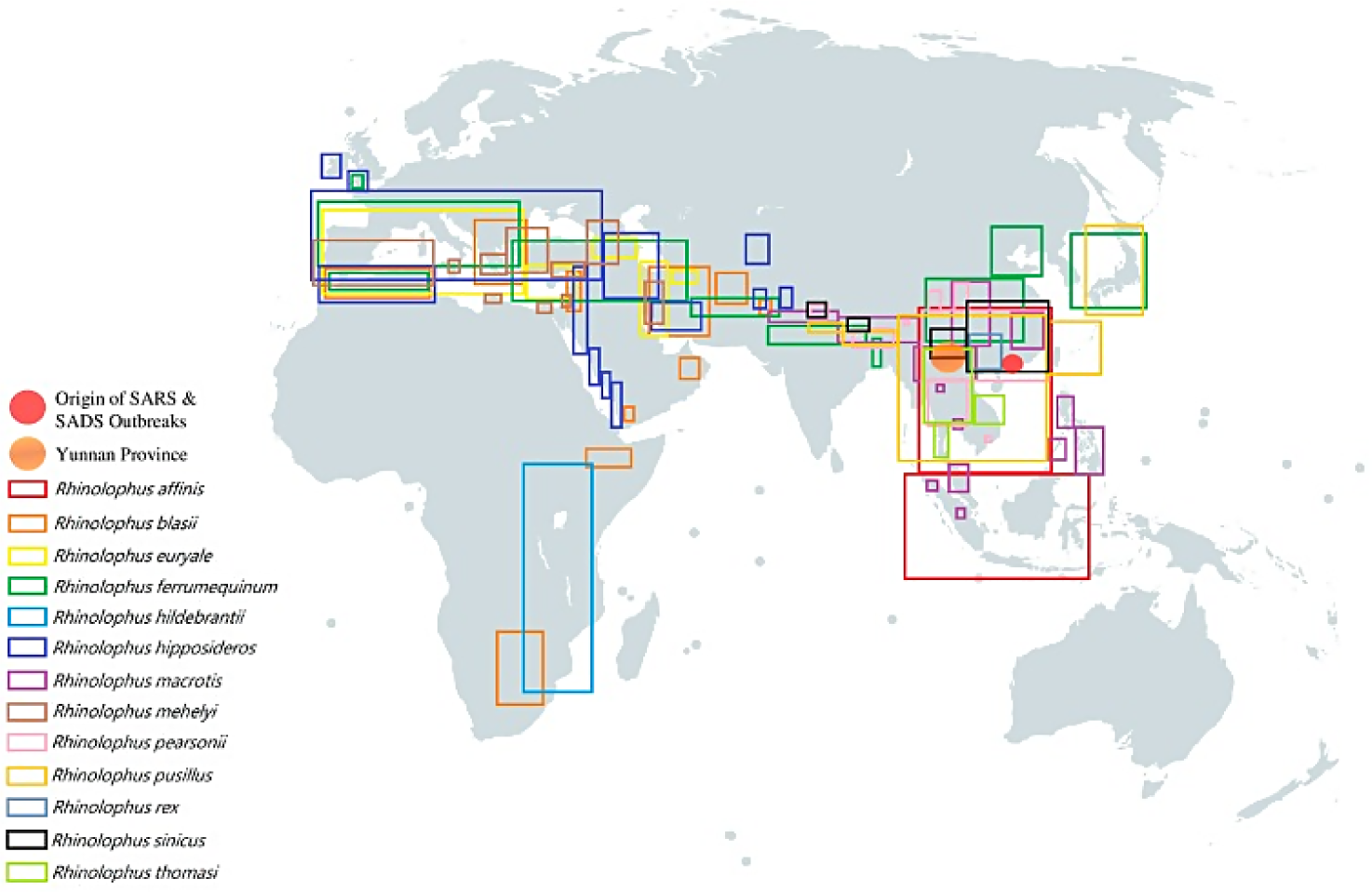
При сравнении коэффициента летальности COVID-19 по данным Центра доказательной медицины CEBM (Centre for Evidence-Based Medicine) (Таблица 1) с картой распространения летучих мышей рода Rhinolophus, переносящих SARS-CoV-1-подобные вирусы, видно, что в таких странах, как Испания, Франция, Италия, Нидерланды, Великобритания, где распространены данные летучие мыши, наблюдается повышенная смертность от COVID-19 c коэффициентом летальности выше 10 [56]. В странах, где не выявлены летучие мыши рода Rhinolophus – носители SARS-CoV-1-подобных вирусов, смертность значи-тельно ниже (коэффициент летальности 4-6). Таким образом, прослеживается прямая корреляция между распространением летучих мышей – носителей SARS-CoV-1-подобных вирусов – и тяжестью инфекции, вызванной новым вирусом SARS-CoV-2. Среди стран Северной Европы выделяется Швеция, в которой не выявлены летучие мыши – переносчики коронавирусов, но наблюдается высокая смертность с коэффициентом летальности 12. Объяснением может служить недавно опубликованная информация о том, что в Швеции гибель людей наблюдается в основном среди иммигрантов из Сирии, Ирака и Афганистана – стран, входящих в пояс распространения летучих мышей – переносчиков SARS-CoV-1-подобных вирусов [57]. Похожая ситуация отмечена в Великобритании, где представители национальных меньшинств погибают от коронавирусной инфекции на 27% чаще, чем основное население Великобритании [58]. Необходимо отметить, что в отдельных районах Великобритании также встречаются летучие мыши рода Rhinolophus, переносящие SARS-CoV-1-подобные коронавирусы.
| Страна | Число летальных случаев | Общее число инфицированных | Коэффициент летальности |
|---|---|---|---|
| Бельгия | 7844 | 49906 | 15.72 |
| Великобритания | 28446 | 186599 | 15.24 |
| Франция | 24895 | 168693 | 14.76 |
| Италия | 28884 | 210717 | 13.71 |
| Нидерланды | 5056 | 40571 | 12.46 |
| Швеция | 2679 | 22317 | 12.00 |
| Венгрия | 351 | 3035 | 11.57 |
| Испания | 25364 | 247122 | 10.22 |
| Индонезия | 845 | 11192 | 7.55 |
| Словения | 96 | 1439 | 6.67 |
| Египет | 429 | 6465 | 6.64 |
| Филиппины | 623 | 9485 | 6.57 |
| Иран | 6203 | 97424 | 6.37 |
| США | 68602 | 1188421 | 5.77 |
| Китай | 4633 | 82880 | 5.59 |
| Дания | 484 | 9670 | 5.01 |
| Швейцария | 1473 | 29905 | 4.93 |
| Польша | 683 | 13937 | 4.90 |
| Финляндия | 230 | 5254 | 4.38 |
| Германия | 6866 | 165664 | 4.14 |
| Австрия | 598 | 15597 | 3.83 |
| Япония | 487 | 14877 | 3.27 |
| Эстония | 55 | 1703 | 3.23 |
Неравномерность распределения смертности при COVID-19 в различных странах может объясняться многими причинами, включая наличие BCG вакцинации [59],дефицитом витамина D [60],а также социальными причинами. Однако выдвинутая нами гипотеза о корреляции плотности популяции летучих мышей, являющихся природным резервуаром различных ко-ронавирусов и, в частности, бетакоронавирусов, близких по антигенным свойствам вирусу SARS-CoV-2, со смертностью от COVID-19 в отдельных странах также заслуживает пристального изучения. Контакты людей и летучих мышей в странах, отличающихся высокой плотностью последних, могут приводить к повторя-ющейся бессимптомной инфекции в течение жизни отдельного человека. Вероятность такого инфициро-вания низкая для детей и молодых людей и повышается с увеличением возраста, что согласуется с данными о меньшем числе смертельных случаев у людей в возрасте до 20 лет при одинаковой частоте заболе-ваний в разных возрастных группах. Возникающие в результате этого процесса В-клетки памяти могут приводить к ускоренной продукции антител при по-следующей инфекции SARS-CoV-2. Раннее появление низкоаффинных антител при COVID-19 может прово-цировать инфицирование макрофагов и гипервоспа-лительный ответ системы врожденного иммунитета. Таким образом, наличие предшествующего иммунитета к коронавирусам может иметь повреждающий эффект у отдельных пациентов пропорционально наличию у них В-клеток памяти к родственным анти-генам. Исследование наличия В-клеток памяти к ан-тигенам бетакоронавирусов у здоровых людей может оказаться способом оценки риска тяжелого течения заболевания при инфекции SARS-CoV-2.


