ВВЕДЕНИЕ
С 2011 года Россия входит в тройку крупнейших ми-ровых экспортеров продукции зерновых культур, в частности пшеницы и ячменя [1]. В каждой стране, закупающей российское зерно, существуют требования, предъявляемые к качеству ввозимых зерновых культур. Особое внимание уделяется фитосанитарному состоянию зерна. Организации по карантину и защите растений в разных странах имеют перечни вредных организмов, рекомендованных для регулирования в качестве карантинных вредных организмов. Список А1 перечня включает карантинные вредные организмы, отсутствующие в данной зоне, а список А2 – карантинные вредные организмы, присутствующие в данной зоне, но не широко распространенные и служащие объектом официальной борьбы. В Европе такой надзор осуществляет Европейская и Средиземноморская организация по карантину и защите растений (European and Mediterranean Plant Protection organization, EPPO) [2]. В большинстве стран-импортеров российской продукции зерновых культур имеется перечень микроорганизмов, содержание которых в зерне не допускается. Следует отметить, что при указании таксономических названий бактерий могут использоваться синонимы, что затрудняет работу фитосанитарных служб. В перечень бактериальных возбудителей болезней зерновых культур, относящихся к родам Triticum L. (пшеница) и Hordeum L. (ячмень) семейства Poaceae (злаки), включены следующие виды:
Pectobacterium rhapontici (Millard 1924) Patel & Kulkarni 1951, возбудитель розового бактериоза зерна пшеницы и ржи. Синонимы: Erwinia rhapontici (Millard 1924) Burkholder 1948 [3], Erwinia carotovora var. rhapontici (Millard) Dye [3]. Этот фитопатоген до настоящего времени не описан на территории Российской Федерации (РФ). Зерновые культуры не являются основными растениями-хозяевами данной бактерии, тем не менее, P. rhapontici входит в карантинный перечень стран Восточной и Южной Африки (подкарантинная продукция – пшеница) [2];
Rathayibacter tritici (Carlson & Vidaver) Zgurskaya, Evtushenko, Akimov & Kalakoutskii, возбудитель желтого слизистого бактериоза пшеницы. Си-нонимы: Clavibacter tritici (Carlson & Vidaver) Davis, Gillaspie, Vidaver & Harris, Corynebacterium michiganense pv. tritici (Hutchinson) Dye & Kemp, Corynebacterium tritici (Hutchinson) Burkholder, Phytomonas tritici (Hutchinson) Bergey, Pseudomonas tritici Hutchinson [2]. Бактерия поражает пшеницу [4] и входит в перечень карантинных видов (список А1) в Бразилии, Узбекистане, Греции, Молдавии и странах ЕАЭС, а также находится в карантинном перечне США [2] и Народной Республики Бангладеш [5];
Pseudomonas fuscovaginae (ex Tanii et al. 1976) Miyajima et al. 1983 [3], возбудитель бурой гнили листовой оболочки злаковых культур. Поражает в основном пшеницу, однако в настоящее время считается растительным патогеном и для других злаков, включая кукурузу и сорго [6]. Бактерия на-ходится в списке A1 Египта [7], а также является карантинным видом в Нигерии. Микроорганизм распространен на территории Азии (Япония, Китай, Малайзия, Иран, Филиппины, Непал), Океании (Австралия), Южной Америки (Бразилия), Северной Америки (Мексика) и Африки (Бурунди и Мадагаскар) [8]. Информация о распространении на территории РФ отсутствует.
Pseudomonas syringae pv. atrofaciens (McCulloch) Young, Dye & Wilkie [2], возбудитель базального бактериоза пшеницы. Синоним– Pseudomonas atrofaciens (McCulloch) Stevens. В природных условиях, кроме пшеницы, фитопатоген поражает рожь, ячмень и овес. Данные о распространении на территории РФ отсутствуют. Возбудитель является карантинным видом в Мексике [2] и Египте [7].
Pseudomonas syringae pv. coronafaciens (Elliott) Young, Dye & Wilkie, возбудитель ореольного бактериоза ржи. Бактерия может поражать также овес. В фитосанитарных требованиях странимпортеров подкарантинной продукцией для данного фитопатогена является пшеница. Карантинный вид в Нигерии и Мексике, входит в перечень ограниченно распространенных карантинных видов (список A2) в Восточной и Южной Африке. Бактерия распространена на территории РФ [2].
Acidovorax avenae subsp. avenae (Manns 1909) Willems et al. 1992 [9], возбудитель бактериальной полосатости листьев. Синонимы: Pseudomonas avenae subsp. avenae Manns 1909, Acidovorax avenae (Manns) Willems, Goor, Thielemans, Gillis, Kersters & De Ley. Бактерия может вызывать болезни у многих растений, имеющих экономическое значение, включая рис, кукурузу, овес, сахарный тростник, просо и лисохвост [10, 11]. Карантинный вид в Египте [7] и Марокко, входит в список A2 в Восточной и Южной Африке, при этом подкарантинной продукцией является пшеница. Считается, что на территории РФ бактерия отсутствует [2];
Xanthomonas translucens pv. cerealis (Hagborg) Vauterin, Hoste, Kersters & Swings, возбудитель черного бактериоза ржи. Синонимы: Xanthomonas campestris pv. cerealis (Hagborg) Dye, Xanthomonas translucens f. sp. cereal Hagborg. Поражает такие злаки, как пшеница, рожь, ячмень и овес. Точные данные о распространении в РФ отсутствуют. Карантинный вид в Мексике [2];
Xanthomonas translucens pv. translucens (Jones, Johnson & Reddy) Vauterin,Hoste, Kersters & Swings, возбудитель черного бактериоза ячменя. Название этой бактерии имеет множество синонимов: Pseudomonas translucens (Jones, Johnson & Reddy) Stapp, Xanthomonas campestris pv. hordei (Hagborg) Dye, Xanthomonas campestris pv. translucens (Jones, Johnson & Reddy) Dye, Xanthomonas translucens (Jones, Johnson & Reddy) Vauterin, Hoste, Kersters & Swings, Xanthomonas translucens pv. hordei (Hagborg) Dye. Основным растением-хозяином является ячмень. Патоген может поражать рожь и пшеницу, а также травы: тимофеевку луговую, бромус и пырей ползучий. Считается, что бакте-рия распространена на территории РФ. Карантинный вид в Марокко и Нигерии, входит в список A2 в Иордании и Турции [2];
Xanthomonas translucens pv. graminis (Egli, Goto & Schmidt) Vauterin, Hoste, Kersters & Swings, возбудитель бактериального увядания зерновых культур. Синонимы: Xanthomonas campestris pv. graminis (Egli, Goto & Schmidt) Dye, Xanthomonas graminis Egli, Goto & Schmid. Поражает злаки, включая пшеницу, рожь и ячмень. Из дикорастущих видов может поражать ежу сборную. Фитопатоген встречается в Европе (Франция, Германия, Швейцария, Великобритания) [2]. Точные данные о распространении на территории РФ отсутству-ют. Карантинный вид в Египте [7];
Xanthomonas translucens pv. undulosa (Smith, Jones & Reddy) Vauterin, Hoste, Kersters & Swings [2], возбудитель черного бактериоза пшеницы. Синонимы: Phytomonas translucens var. undulosa Stapp, Xanthomonas campestris pv. undulosa (Smith, Jones & Reddy) Dye, Xanthomonas translucens f. sp. undulosa. Считается, что патоген распространен по всему миру, поражает пшеницу и ячмень [12]. Входит в карантинный перечень Нигерии.
Rathayibacter rathayi (Smith) Zgurskaya, Evtushenko, Akimov & Kalakoutskii, смолистый бактериоз. Синонимы: Corynebacterium michiganense pv. rathayi (Smith) Dye & Kemp, Corynebacterium rathayi (Smith) Dowson, Phytomonas rathayi (Smith) Bergey et al. Бактерия поражает рожь, пшеницу, а также ежу сборную. Данный вид распространен во многих странах Европы (Австрия, Кипр, Дания, Германия, Норвегия, Румыния, Швеция, Великобритания), однако считается, что в РФ он отсутствует. Входит в список A1 в странах Южной Африки [2].
Pseudomonas cichorii (Swingle) Stapp, возбудитель бактериального ожога различных сельскохозяйственных культур. В большей степени поражает салат [13], однако для стран-импортеров под-карантинной продукцией является в том числе и пшеница [7]. Синонимы: Phytomonas cichorii, Pseudomonas endiviae, Pseudomonas papaveris. Бактерия широко распространена на всех континентах. Входит в карантинный перечень Мексики, в список А1 в Египте и А2 – в Иордании [2].
Возбудители бактериозов зерновых культур, кроме Rathayibacter tritici, не являются карантинными видами в РФ, в связи с чем исследования с целью их выявления не проводились, и достоверные данные об их распространении на территории РФ отсутствуют. Кроме того, отсутствует методика диагностики ряда бактериальных фитопатогенов зерновых культур. Соответственно, выявление возбудителей бактериозов (за исключением Rathayibacter tritici) в партиях как экспортируемого, так и импортируемого зерна в РФ на сегодняшний день не проводится, что приводит к высокому риску проникновения на территорию РФ фитопатогенов, способных нанести существенный экономический вред сельскому хозяйству.
Таким образом, разработка методов диагностики фитопатогенов зерновых культур является актуальной задачей.
Цель настоящего исследования состояла в выделении и идентификации возбудителей бактериальных болезней пшеницы и ячменя для установления фитосанитарного состояния российской продукции зерновых культур.
МАТЕРИАЛЫ И МЕТОДЫ
Сбор материала
Всего было обследовано 1720 га посевных площадей, из них 1536 га – озимая пшеница, 184 га – ячмень. Во время проведения обследования растения озимой пшеницы и ячменя находились в фазе колошения. В первую очередь осматривали растения с симптомами пятнистости, наличия штрихов и полос, а также признаков увядания и деформации листьев. Подобные симптомы встречаются, например, при заболеваниях, вызванных бактериями Pseudomonas syringae pvs. Обращали также внимание на наличие тли, которая является потенциальным переносчиком бактерий Xanthomonas translucens pvs. [14]. Осо-бое внимание уделяли растениям с наличием гнили и хлоротично-некротичными полосами на листьях, так как подобные симптомы могут быть вызваны X. translucens pv. translucens [15]. Растения с механическими повреждениями также отмечали, поскольку повреждения могут способствовать проникновению патогенных бактерий, например, X. translucens pv. graminis, в ткани протоксилемы, откуда возбудитель впоследствии мигрирует в сосудистую ткань [16]. С каждого участка отбирали один образец вегета-тивных частей растений зерновых культур с соот-ветствующими симптомами, добавляя при этом к образцу достаточное количество здоровой ткани тех же растений. Сбор и упаковка образцов были организованы так, чтобы предотвратить повреждения, контакт с другими образцами и контаминацию. Листья и стебли перекладывали фильтровальной бумагой и помещали в контейнеры с отверстиями для доступа воздуха. До проведения исследования образцы хранили при температуре от 2 до 8°C.
Подготовка аналитических проб
В лаборатории получали суспензии микробиоты образцов (аналитические пробы). Отбор проб проводили из участков на стыке симптоматической и здоровой тканей. От каждого образца отбирали лабораторную пробу массой от 1.0 до 2.5 г и помещали в емкость объемом 100 мл. Взвешивание проб проводили на лабораторных электронных весах (AJH-4200CE, Vibra, Япония). К лабораторным пробам добавляли фосфатно-солевой буфер (PBS) [17] в соотношении 20:1, после чего пробы подвергали интенсивному встряхиванию на ротационном шейкере Unimax 2010 (Heidolph, Германия) при режиме 200 об/мин в течение 45-60 мин. Экстракт отделяли от примесей растительных тканей безнапорной фильтрацией с использованием фильтров обеззоленных «Синяя лента», размер пор 3-5 мкм. Полученные экстракты центрифугировали 10 мин при 4°C (10 000 g, Allegra X-30R, Beckman Coulter, Дания). Сразу после центрифугирования супернатант удаляли, а осадок ресуспендировали в 1 мл PBS. Полученную суспензию использовали для выделения бактерий.
Изоляция бактерий
Выделение культур проводили на средах CRL, CRL.2 и mCRL.2. Среда CRL содержала следующие компоненты: пептон 12.0 г, глицерин 10.0 г, агар 18.0 г, MgSO4 0.7 г, K2HPO4 2.0 г, KH2PO4 2.0 г, глюкозу 2.5 г, дрожжевой экстракт 2.0 г, мясной пептон 2.0 г, сахарозу 15.0 г, NaCl 2.0 г, CaCO3 20.0 г (реактивы про-изводства PanReac AppliChem, Испания) на 1 л дис-тиллированной воды. Среда CRL.2 состояла из тех же компонентов, за исключением CaCO3. Все ингре-диенты перемешивали, доводили рН 20%-м раствором соляной кислоты до 7,0-7,2 с помощью pH-метра (МР 220, Mettler Toledo, Швейцария) и стерилизовали при температуре 121°C в течение 15 мин (автоклав MLS-3020U, Sanyo, Япония). Для получения среды mCRL.2 к среде CRL.2 после стерилизации и охлаждения до 50°C добавляли спиртовой (70%) раствор ци-клогексимида до его конечной концентрации 200 мг на 1 л среды и водный раствор 2,3,5-трифенилтетразолия хлористого (ТТХ) до конечной концентрации 50 мг на 1 л среды.
Аналитические пробы использовали для приготовления серии десятикратных разведений в PBS. Разведения 10-3 и 10-4 в объеме 100 мкл высевали с помощью шпателя Дригальского на чашки Петри со средой mCRL.2, используя метод растяжения на 2 чашки в двух повторах (4 чашки на каждый образец). После посева чашки Петри плотно оборачивали герметизирующей пленкой «Parafilm» и выдерживали при температуре +25°C в инкубаторе (MIR-254, Panasonic Healthcare Co., Япония) в течение пяти суток. По истечении этого срока проводили отбор колоний различных морфотипов. Отдельные колонии пересевали на чашки Петри со средами CRL и CRL.2 с помощью бактериологической петли для получения чистой культуры бактерий. Чашки, обернутые пленкой «Parafilm», инкубировали при температуре +25°C в течение 72 ч. Затем с помощью бактериологической петли отбирали отдельные колонии и помещали в микропробирки с 200 мкл PBS.
ПЦР и секвенирование
Для лизирования клеток пробы инкубировали 10 мин при 96°C, после чего охлаждали в морозильной камере в течение 5 мин. Полученный препарат использовали для проведения ПЦР, которую проводили в несколько этапов. На первом этапе ДНК всех изолятов тестировали методом классической ПЦР с праймерами PSF/PSR (PSF 5’-AGC CGT AGG GGA ACC TGC GG-’3, PSR 5’-TGA CTG CCA AGG CAT CCA CC-’3), специфич-ными к роду Pseudomonas. В качестве положительного контроля использовали штаммы Pseudomonas syringae pv. syringae, полученные из венгерской коллекции AOBC PPSCD. Для приготовления реакционной смеси на одну реакцию использовали 16.0 мкл деионизированной воды, 5.0 мкл мастер-микс 5X MasDDTaqMIX-2025 (ЗАО «Диалат», Россия) и по 1.0 мкл каждого праймера в концентрации 10 пмоль. Для проведения реакции использовали 2 мкл ДНК. Итоговый объем – 25 мкл. Амплификацию проводили в следующем режиме: начальная денатурация 95°C – 10 мин, затем 25 циклов: 95°C– 20 с, 64°C– 15 с, 72°C– 15 с; финальная элонгация 72°C– 2 мин.
Изоляты, отрицательные в ПЦР с праймерами PSF/PSR, тестировали повторно в ПЦР с универсальными праймерами 8UA/519B, специфичными к участку 16S-23S рибосомальной РНК (рРНК) (8UA: 5’-AGA GTT TGA TCM TGG CTC AG-3’, 519B: 5’-GTA TTA CCG CGG CKG CTG-3’). Размер продукта амплификации – 500 п.о. Праймеры заказывали в ООО «Евроген» (РФ). Для приготовления реакционной смеси для одного образца использовали 14 мкл деионизированной воды, 5 мкл мастер-микс 5X MasDDTaqMIX-2025 (ЗАО «Диалат», РФ), по 2 мкл каждого праймера в концентрации 10 пмоль. Затем в микропробирку вносили 2 мкл ДНК-матрицы образца. Итоговый объ-ем –25 мкл. Режим амплификации: начальная денату-рация 96°C– 10 мин, затем 35 циклов: 95°C– 15 с, 55°C – 30 с, 72°C– 30 с; финальная элонгация 72°C– 10 мин.
Изоляты, положительные в тесте с праймерами PSF/PSR, далее анализировали с праймерами SyD1/ SyD2 (SyD1 5’-CAGCGGCGTTGCGTCCATTGC-3’, SyD2 5’-TGCCGCCGACGATGTAGACCAGC-3’), специфичными к Pseudomonas syringae pv. syringae. В качестве положительного контроля также использовали штаммы Pseudomonas syringae pv. syringae. Для приготовления реакционной смеси для одной реакции использовали 17.4 мкл деионизированной воды, 5 мкл мастер-микс 5X MasDDTaqMIX-2025 (ЗАО «Диалат», Россия), по 0.3 мкл каждого праймера в концентрации 10 пмоль. В каждую пробирку вносили 2 мкл ДНК образца. Итоговый объем – 25 мкл. Программа амплификации: начальная денатурация 95°C – 10 мин, затем 25 циклов: 95°C – 20 с, 64°C – 15 с, 72°C – 45 с; финальная элонгация 72°C– 7 мин.
Для проведения всех ПЦР-реакций использовали амплификатор Bio-Rad T100 Thermal Cycler (Bio-Rad, США). Определение продуктов реакции проводили в 1.5%-м агарозном геле, используя источник питания для электрофореза Power Pac HV и Bio-Rad Imaging System (Bio-Rad, США).
Для каждого образца, положительного в одном из тестов, проводили идентификацию методом секвенирования по Сэнгеру [18]. Для этого ампликоны, полученные методом ПЦР, очищали при помощи DNA Purification Kit (Thermo Fisher Scientific, США) согласно инструкции производителя. Затем в каждом образце, содержащем очищенные ампликоны, проводили измерение концентрации ДНК, используя спектрофотометр NanoDrop-2000 (Thermo Fisher Scientific, США). Концентрацию ДНК каждого образца доводили до рабочей, исходя из длины продукта амплификации на электрофореграмме (длина продукта, деленная на 100). Для разведения использовали воду. Затем проводили амплификацию, используя набор Big Dye Kit (Thermo Fisher Scientific, США); данный набор содержит меченые dNTP для получения меченой цепи. Состав реакционной смеси для одной реакции: 1 мкл Big Dye 3.1, 1.5 мкл Big Dye buffer, 2 мкл праймера (прямого или обратного) в концентрации 0.8 пмоль, 4.5 мкл воды, 1 мкл ДНК. Режим амплифи-кации: 96°C– 1 мин, затем 25 циклов 96°C– 10 с, 50°C – 5 с, 60°C – 4 мин. После амплификации очищали ДНК, используя BigDyeョ XTerminator™ Purification Kit (Thermo Fisher Scientific, США) согласно инструкции производителя. Затем по 25 мкл очищенной ДНК вносили в лунки секвенатора АВ-3500 (Applied Biosystems, США). Программу секвенирования выбирали исходя из длины фрагментов. Результаты обрабатывали с помощью программы BioEdit. Полученные нуклеотидные последовательности сравнивали с последовательностями бактерий, размещенными в GenBank, с помощью сервиса BLAST [19].
РЕЗУЛЬТАТЫ
Идентификация бактериальных изолятов
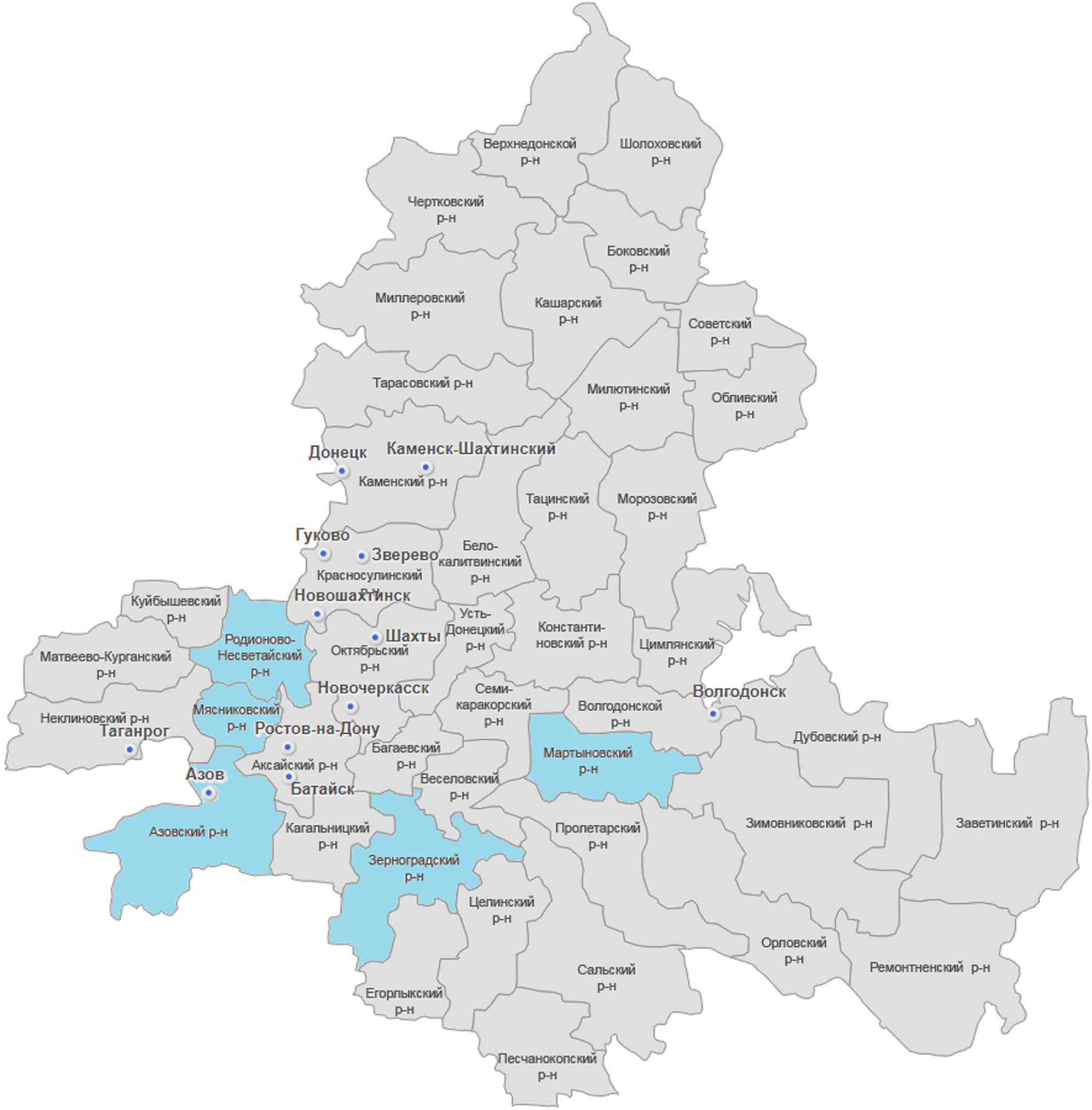
Объектами исследования являлись бактериальные изоляты, выделенные из образцов пшеницы и ячменя. Отбор образцов растительного материала проводили в мае 2019 года в Родионово-Несветайском, Мясниковском, Зерноградском, Азовском и Мартыновском районах Ростовской области (Рис. 1). Отбирали растения с симптомами заболевания (пятнистость, наличие штрихов и полос) (Рис. 2). Информация об обследованных сортах с указанием площадей под посевами представлена в Таблице 1. Всего было отобрано 22 образца. В процессе выделения бактериальных культур на питательной среде mCRL.2 были получены колонии различных морфотипов (Рис. 3). Для ПЦР-тестов и идентификации было отобрано 116 колоний.
| Район | Культура | Сорт | Площадь (га) |
|---|---|---|---|
| Родионово-Несветайский | Ячмень яровой | Леон | 18 |
| Пшеница озимая | Калым | 47 | |
| Алексеич | 50 | ||
| Тарасовская 70 | 57 | ||
| Мясниковский | Пшеница озимая | Безостая 100 | 168 |
| Калым | 146 | ||
| Лидия | 90 | ||
| Баграт | 88 | ||
| Ячмень озимый | Достойный | 15 | |
| Эспада | 15 | ||
| Зерноградский | Пшеница озимая | Табор | 100 |
| Танаис | 81 | ||
| Таня | 252 | ||
| Табор | 114 | ||
| Баграт | 110 | ||
| Азовский | Пшеница озимая | Сила | 69 |
| Васса | 42 | ||
| Стан | 46 | ||
| Юкка | 42 | ||
| Гром | 16 | ||
| Ячмень озимый | Тимофей | 136 | |
| Мартыновский | Пшеница озимая | Баграт | 18 |

Чтобы выбрать изоляты, принадлежащие роду Pseudomonas, ДНК всех изолятов тестировали методом ПЦР с праймерами PSF/PSR, специфичными к данному роду [20]. В результате тестирования были получены продукты амплификации длиной от 420 до 750 п.о. для 43 образцов ДНК бактериальных изолятов из 116 (Рис. 4А). В 31 случае из 43 длина продукта амплификации составляла 600 п.о., что соответствовало положительному контролю (Рис. 4Б).
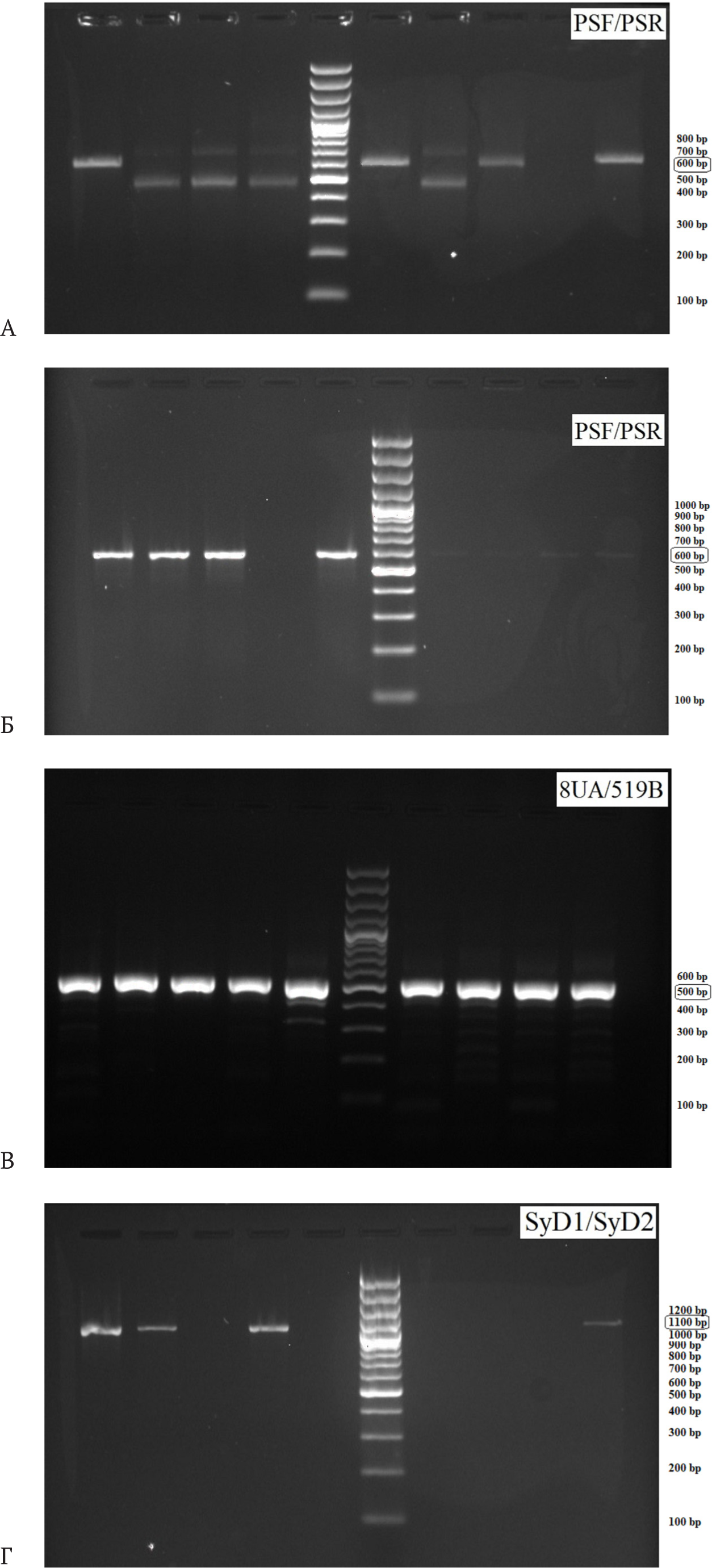
Пробы, выделенные из 73 бактериальных изолятов, показавших отрицательный результат при тестировании с праймерами PSF/PSR, далее анализировали в ПЦР с универсальными праймерами 8UA/519B, специфичными к участку 18S-23S рРНК [21]. Полученные продукты амплификации имели длину 500 п.о. (Рис. 4В). Пробы, выделенные из 43 бактериальных изолятов, положительных при тестировании с праймерами PSF/PSR, далее анализировали с праймерами SyD1/SyD2, специфичными к Pseudomonas syringae pv. syringae [20]. В результате были получены фрагменты длиной 1100 п.о., соответствующие положительному контролю, для 7 образцов (Рис. 4Г).
Таким образом, для идентификации методом сек-венирования было получено 43 образца продуктов амплификации с праймерами PSF/PSR, 73 – с праймерами 8UA/519B и 7 – с праймерами SyD1/SyD2. Результаты изучения состава бактериальных изолятов, идентифицированных методом секвенирования указанных продуктов амплификации, представлены в Таблице 2.
| Культура | Сорт | Бактерии, идентифицированные в ПЦР с соответствующими праймерами | ||
|---|---|---|---|---|
| PSF/PSR | 8UA/519B | SyD1/SyD2 | ||
| Ячмень яровой | Леон | Pseudomonas sp. |
Pantoea agglomerans, Enterobacteriaceae, Paenibacillus, Stenotrophomonas, Bacillus sp., Erwinia sp., Pantoea sp. |
P. syringae pv. syringae, P. syringae pv. atrofaciens |
| Пшеница озимая | Калым |
Paenibacillus, Stenotrophomonas, Bacillus sp., Erwinia sp., Pantoea sp. | ||
| Алексеич |
P. fluorescens, P. poae, Pseudomonas sp. | |||
| Тарасовская 70 | Pseudomonas sp. | |||
| Пшеница озимая | Безостая 100 | Pseudomonas sp. | Paenibacillus, Stenotrophomonas, Bacillus sp., Erwinia sp., Pantoea sp. | |
| Калым |
Curtobacterium sp., Pseudomonas sp. | |||
| Лидия | Pseudomonas sp. | |||
| Баграт | ||||
| Ячмень озимый | Достойный | Pseudomonas sp. | ||
| Эспада | ||||
| Пшеница озимая | Табор |
P. fluorescens, Pseudomonas sp. |
Paenibacillus, Stenotrophomonas, Bacillus sp., Erwinia sp., Pantoea sp. | |
| Танаис | Pseudomonas sp. | |||
| Таня | ||||
| Табор |
P. fluorescens, Pseudomonas sp. | |||
| Баграт | Pseudomonas sp. | |||
| Пшеница озимая | Сила | Pseudomonas sp. |
Paenibacillus, Stenotrophomonas, Bacillus sp., Erwinia sp., Pantoea sp. | |
| Васса | ||||
| Стан | ||||
| Юкка |
P. hibiscicola, Pseudomonas sp. | |||
| Гром | Pseudomonas sp. | |||
| Ячмень озимый | Тимофей |
P. azotoformans, Pseudomonas sp. |
Paenibacillus, Stenotrophomonas, Bacillus sp., Erwinia sp., Pantoea sp. | |
| Пшеница озимая | Баграт | Pseudomonas sp. |
Paenibacillus, Stenotrophomonas, Bacillus sp., Erwinia sp., Pantoea sp. | |
В результате секвенирования продуктов ампли-фикации с праймерами PSF/PSR идентифицированы следующие бактериальные изоляты:
Pseudomonas fluorescens (из образца озимой пшеницы сорта Алексеич Родионово-Несветайского района, а также образца озимой пшеницы сорта Табор Зерноградского района). Колонии бактерии на питательной среде mCRL.2 были круглые с неровными краями, 0.02 мм в диаметре, белого цвета;
P. poae (из образца озимой пшеницы сорта Алексеич). Культура на среде mCRL.2 представляла собой круглые колонии правильной формы розового цвета, 0.05 мм в диаметре.
Curtobacterium sp. (из образца озимой пшеницы сорта Калым Мясниковского района). Культура на среде CRL.2 имела плоские желто-бежевые колонии неровной формы, 1.0 мм в диаметре. На среде CRL колонии были ярко-оранжевого цвета;
P. azotoformans (из образца озимого ячменя сорта Тимофей Азовского района). На среде CRL колонии бактерии были молочно-белые, неровной формы, выпуклые, до 5.0 мм в диаметре;
P. hibiscicola (из образца озимой пшеницы сорта Юкка Азовского района). На среде CRL колонии культуры были матовые, кремово-желтые, выпуклые, круглые с ровными краями, от 1.0 до 5.0 мм в диаметре.
Другие продукты амплификации, полученные с праймерами PSF/PSR, путем сравнения с последо-вательностями, размещенными в GenBank, иденти-фицированы как Pseudomonas sp.
В процессе анализа нуклеотидных последователь-ностей, полученных после амплификации с праймерами 8UA/519B, были идентифицированы следующие изоляты:
Pantoea agglomerans (из образца ярового ячменя сорта Леон Родионово-Несветайского района). Колонии данного изолята на среде mCRL.2 были круглые, 4 мм в диаметре, персикового цвета с ярко-малиновым центром. На средах CRL.2 и CRL культура имела колонии желтого цвета, неровные, растекающиеся;
Enterobacteriaceae (из образца ярового ячменя сорта Леон). На среде mCRL.2 культура имела круглые слабовыпуклые колонии малинового цвета, 3.0 мм в диаметре.
Также во всех образцах пшеницы и ячменя были идентифицированы изоляты, относящиеся к бактериям Paenibacillus, Stenotrophomonas, Bacillus sp., Erwinia sp. и Pantoea sp.
В результате секвенирования продуктов амплифи-кации, полученных с праймерами SyD1/SyD2, были идентифицированы изоляты Pseudomonas syringae pv. syringae и Pseudomonas syringae pv. atrofaciens в образцах ярового ячменя сорта Леон Родионово-Несветайского района и озимой пшеницы сорта Калым Мясниковского района. На средах CRL.2 и CRL культуры данных изолятов имели белые, матовые, растекающиеся колонии неровной формы, характеризующиеся быстрым агрессивным ростом (Рис. 5).
ОБСУЖДЕНИЕ
В данном исследовании проведено выделение и идентификация возбудителей бактериальных болезней пшеницы и ячменя. В процессе проведения обследований посевов и сбора образцов озимой пшеницы и ячменя в Родионово-Несветайском, Мясниковском, Зерноградском, Азовском и Мартыновском районах Ростовской области на растениях было отмечено на-личие симптомов бактериальных болезней, таких как полосы, пятнистости, хлоротичные и некротические участки тканей. Данные наблюдения позволяют сделать вывод о присутствии на посевах зерновых культур в Ростовской области бактериальных фитопатогенов с высокой вирулентностью.
Для посева бактериальных суспензий использовались три экспериментальные питательные среды. На всех средах отмечался быстрый рост бактерий. Ис-пользование среды mCRL.2, содержащей циклогек-симид, позволило избежать зарастания чашек Петри колониями грибов при посеве. При этом данное про-тивомикробное вещество не проявляло бактериоста-тических свойств, что позволило провести выделение максимального числа различных бактерий. Другой компонент среды – водный раствор 2,3,5-трифенил-тетразолия хлористого в концентрации 50 мг/л – по-зволил окрасить некоторые бактериальные колонии, что упростило описание их морфологии. Использование для культивирования чистых культур сред CRL.2 и CRL показало их перспективность при работе с воз-будителями бактериозов зерновых культур.
В процессе проведения ПЦР-теста с праймерами PSF/PSR не были получены продукты реакции длиной 752 п.о., описанные разработчиками праймеров [17]. Данная ПЦР позволяет получать продукты амплифи-кации длиной от 420 до 750 п.о. с различными видами бактерий рода Pseudomonas. Размер продукта амплификации для положительного контроля ПЦР, P. syringae pv. syringae, составил 600 п.о. В рамках данного исследования идентифицированы бактерии Pseudomonas azotoformans, P. poae, P. hibiscicola и P. fluorescens. Данный тест можно использовать в качестве метода определения псевдомонад среди отобранных колоний.
Использование праймеров 8UA/519B с последующим секвенированием позволило провести идентификацию бактерий, принадлежащих различным родам, таким как Curtobacterium sp., Enterobacteriaceae, Pantoea agglomerans, Stenotrophomonas, Paenibacillus, Bacillus sp., Erwinia sp. и Pantoea sp. Виды, принадле-жащие роду Pseudomonas, с помощью данных праймеров идентифицировать не удалось, так как участок генома, который является мишенью, идентичен у большинства псевдомонад.
Амплификация с ДНК бактерий, принадлежащих виду P. syringae pv. atrofaciens, с праймерами SyD1/SyD2, по данным литературы [17], должна приводить к образованию продукта реакции длиной 558 п.о., однако мы установили, что размер продукта ПЦР составляет 1100 п.о., в том числе и для положительного контроля, P. syringae pv. syringae, что соответствует расположению данных праймеров на участке-мишени последовательности генома P. syringae (с 2966585 по 2967602 п.о., GenBank CP047267.1). Использование данных праймеров с последующим секвенированием позволило идентифицировать бактерии P. syringae pv. atrofaciens и P. syringae pv. syringae, входящие в карантинные перечни стран-импортеров зерновых культур.
Данные, представленные в Таблице 2, показывают, что каждый образец озимой пшеницы и ячменя содержит в составе своей микробиоты бактерии, принадлежащие родам Pseudomonas, Paenibacillus, Stenotrophomonas, Bacillus, Erwinia и Pantoea. Среди найденных фитопатогенов бактерии Pseudomonas, Erwinia и Pantoea потенциально могут обладать наибольшей вирулентностью, так как именно данные роды бактерий содержат наибольшее число фитопатогенных видов [22]. Это может быть связано с тем, что вышеуказанные бактерии, являясь грамотрицательными, имеют системы секреции, отличные от имеющихся у грамположительных бактерий [23]. Типы секреции III, IV и VI позволяют грамотрицательным бактериям доставлять факторы вирулентности через клеточные мембраны растения-хозяина [24]. Принимая во внимание наличие симптомов бактериальных болезней на посевах озимой пшеницы и ячменя в период проведения обследования, можно предположить, что выделенные изоляты, такие как P. syringae pvs., являются высоковирулентными в отношении растений-хозяев [22].
Виды фитопатогенных бактерий, входящие в карантинные перечни стран-импортеров, за исключением P. syringae pv. atrofaciens и P. syringae pv. syringae, не были обнаружены в исследованных образцах. Использованные методы идентификации могли быть недостаточными для идентификации некоторых псевдомонад, таких как P. cichorii и P. fuscovaginae, так как при сравнении полученных последовательностей нуклеотидов с последовательностями, размещенными в GenBank, ряд бактерий, идентифицированных как бактерии рода Pseudomonas, не определены до вида.
Тем не менее, использованный подход позволяет сделать вывод об отсутствии в отобранных образцах таких бактерий, как Pectobacterium rhapontici, Rathayibacter tritici, R. rathayi, Acidovorax avenae subsp. avenae и Xanthomonas translucens pvs.
Данные о составе микробиоты пшеницы и ячменя, полученные в результате исследования, могут быть использованы для определения соответствия российской продукции зерна фитосанитарным требованиям стран-импортеров.



