ВВЕДЕНИЕ
Процент зараженных зерновок – стандартный показатель, используемый для характеристики микробиологической чистоты зерна. Однако, в зависимости от ряда факторов (культура, устойчивость сорта, время заражения, условия окружающей среды), гриб способен проникать в ткани зерновки на различную глубину и локализоваться в цветковой пленке, в алейроновом слое или полностью заселять эндосперм и зародыш. Поэтому процент зараженного зерна, установленный в результате микологического анализа, как правило, слабо связан со всхожестью зерна и содержанием микотоксинов, продуцируемых грибами [1, 2]. Эта проблема особенно характерна для пленчатых культур (овса и ячменя), у которых цветковая пленка зачастую обильно колонизирована разными видами грибов при низкой зараженности самого зерна. Кроме того, анализ зараженности зерна микробиологическим методом затруднен его длительностью (7–14 суток) и субъективностью получаемых результатов (точность идентификации грибов зависит от опыта исследователя).
Точный количественный анализ присутствия патогенов в зерне и выявление закономерностей заражения ими растений в разных условиях среды (годовые колебания погодных условий, изменения технологии возделывания культур) являются актуальными задачами настоящего времени. К числу современных методов количественного анализа со-держания грибов в зерне относится количественная полимеразная цепная реакция (кПЦР), или ПЦР в реальном времени. При помощи этого метода, основанного на использовании фрагментов ДНК грибов в качестве молекулярных маркеров, можно оценить количество ДНК-мишени патогена или группы сходных патогенов [1, 3-6].
Методы молекулярной биологии позволяют выявить присутствие грибов в образцах растительной ткани, даже если патоген утратил свою жизнеспособность и не был обнаружен традиционным микологическим методом. Количество ДНК гриба, выявленной в образце зерна, зависит от биомассы гриба и является наиболее корректным показателем присутствия патогена в зерне, позволяющим с высокой точностью прогнозировать наличие микотоксинов. Кроме того, метод ПЦР имеет такие неоспоримые преимущества перед микробиологическими методами, как объективность количественной оценки, высокая чувствительность и скорость анализа, а также возможность одновременного анализа большого количества образцов.
Целью исследования являлась адаптация метода количественной ПЦР для оценки содержания ДНК грибов Alternaria Nees, Bipolaris Shoemaker и Fusarium Link, относящихся к наиболее широко распространенным представителям микобиоты зерна.
МАТЕРИАЛЫ И МЕТОДЫ
Образцы зерновых культур
В 2016 г. в поле на территории Волосовского госсортоучастка (Ленинградская область) в конкурсных испытаниях были посеяны зерновые культуры, включающие 10 сортов овса: Аватар (Россия), Боррус (Германия), Всадник (Россия), Залп (Россия), КВС Контендер (Германия), Медведь (Россия), Озон (Германия), Привет (Россия), Стиплер (Россия) и Яков (Россия); 9 сортов пшеницы: Велламо (Россия), Каликсо (Франция), Ленинградская 6 (Россия), Ленинградская 12 (Россия), Ленинградская 97 (Россия), Ликамеро (Франция), Марбл (Канада), Сударыня (Россия) и Тризо (Германия); 12 сортов ячменя: Бенте (Германия), Деспина (Германия), Инари (Финляндия), Криничный (Беларусь), Ленинградский (Россия), Московский 86 (Россия), Норд 132523 (Германия), Олимпик (Франция), Саломе (Германия), Суздалец (Россия), Фэст (Беларусь) и Черио (Германия). Семена высевали без предварительного протравливания, культуры возделывали по принятой на госсортоучастках технологии.
Зерно нового урожая (по 10 г среднего образца каждого сорта) гомогенизировали в стерильных размольных стаканах на мельнице Tube Mill Control (IKA, Германия) в течение 30 с. Скорость размола зерна составляла 20000 об/мин. Размолотую муку хранили при –20℃ до последующей экстракции ДНК (навеска 200 мг) и микотоксинов (навеска 1 г).
Микологический анализ зерна
Для того чтобы выявить основные группы патогенов в микобиоте зерна и целенаправленно определить их содержание с помощью кПЦР, провели микологический анализ зерна шести сортов (по два каждой культуры) на питательной картофельно-сахарозной агаризованной среде (КСА). Из каждого среднего образца отбирали 100-200 зерен, которые поверхностно стерилизовали 5% раствором гипохлорита натрия в течение 1-3 мин. Затем зерна отмывали стерильной водой и раскладывали в чашки Петри на КСА. В питательную среду предварительно вносили 1 мл/л смеси антибиотиков (HyClone™, GE Healthcare Life Sciences, Австрия) для подавления роста бактерий и 0.4 мкл/л раствора Triton X 100 (Panreac, Испания) для снижения линейного роста мицелиальных грибов [2].
Через 7 суток инкубирования чашек Петри в тер-мостате (в темноте, при 24℃) проводили учет чис-ленности и разнообразия грибов. Таксономическую принадлежность выросших микромицетов определяли по сумме макро-и микроморфологических признаков с использованием определителя [7]. Зараженность зерна определенным таксоном рассчитывали как отношение числа зерен, из которых был выделен данный таксон, к общему числу анализируемых зерен, выраженное в процентах.
Выделение ДНК и кПЦР
Выделение ДНК из зерновой муки проводили с помощью набора Genomic DNA Purification Kit (Thermo Fisher Scientific, Литва) согласно адаптированному протоколу. С помощью этого же набора выделяли ДНК из мицелия типовых штаммов грибов Alternaria tenuissima (A. tenuissima) (Nees et T. Nees: Fr.) Wiltshire (MFP556081), B. sorokiniana Shoemaker (MFG59013), F. graminearum Schwabe (MFG58775), F. culmorum (Wm.G. Sm.) Sacc. (MFG102100), F. sporotrichioides Sherb. (MGF163303), выращенных на КСА. Все типовые штаммы грибов хранятся в коллекции лаборатории микологии и фитопатологии ФГБНУ ВИЗР.
Концентрации ДНК, полученной из муки и штаммов, оценивали, используя флуориметр Qubit 2.0 с набором реагентов Quant–iT dsDNA HS Assay Kit (Thermo Fisher Scientific, США). Концентрацию ДНК, выделенной из муки, выравнивали до 2-50 нг/мкл. Исходную ДНК типовых штаммов грибов разбавляли до концентрации 10 нг/мкл и использовали для построения калибровочной кривой в десятикратных последовательных разведениях.
Содержание ДНК грибов Alternaria и F. graminearum оценивали методом кПЦР с зондами TaqMan. Реакцию проводили в объеме 20 мкл, содержащем 10 мкл 2×TaqM мастер-микс (АлкорБио, Россия), 300 нМ каждого праймера, 100 нМ флуоресцентной пробы (Евроген, Россия) и 2 мкл раствора ДНК. Содержание ДНК F. culmorum, F. sporotrichioides и B. sorokiniana определяли с помощью кПЦР с красителем SYBR Green. Реакцию проводили в объеме 20 мкл, содержащем 4 мкл 5×qPCRmix-HS SYBR мастер-микса, 500 нМ каждого праймера (все реактивы – Евроген, Россия) и 2 мкл раствора ДНК. Последовательности праймеров и протоколы амплификации представлены в Таблице 1. Реакции проводили на термоциклере CFX96 Real-Time System (BioRad, США), обработку первичных данных – с помощью программного обеспечения Bio-Rad CFX Manager 1.6.
| Целевой объект | Название праймеров и проб | Последовательность праймеров и проб, 5’– 3’ | Протокол амплификации | Литературный источник |
|---|---|---|---|---|
| F. graminearum | TMFg12f | CTCCGGATATGTTGCGTCAA | 95℃ – 15 мин; [95℃ – 15 с; 60℃ – 60 с]×40 | [1] |
| TMFg12r | CGAAGCATATCCAGATCATCCA | |||
| TMFg12p | FAM-GAGAATGTCTTGAGGCAATGCGAACTTTBHQ1 | |||
| F. culmorum | FculC561f | CACCGTCATTGGTATGTTGTCACT | 50℃ – 2 мин, 95℃ – 10 c, [95℃ – 15 с, 62℃ – 60 с]×40 | [3] |
| FculC614r | CGGGAGCGTCTGATAGTCG | |||
| F. sporotrichioides | PFusf | CCGCGCCCCGTAAAACG | 95℃ – 3 мин, [95℃ – 10 с, 60℃ – 10 с, 72℃ – 20 с]×40 | [8] |
| PSporR | ACTGTGTTTGCACACAGATC | |||
| Alternaria spp. | DirITSAlt | TGTCTTTTGCGTACTTCTTGTTTCCT | 95℃ – 3 мин; [95℃ – 10 с; 60℃ – 60 с; 72℃ – 3 с]×40 | [5, 9] |
| InvITSAlt | CGACTTGTGCTGCGCTC | |||
| AltTM | FAM-AACACCAAGCAAAGCTTGAGGGTACAAAT-TAMRA | |||
| B. sorokiniana | COSA_F | TCAAGCTGACCAAATCACCTTC | 95℃ – 3 мин; [95℃ – 10 с; 68℃ – 20 с; 72℃ – 45 с]×40 | [10], с моди-фикациями |
| COSA_R | CTTCTCACCAGCATCTGAATATATGA |
Количество ДНК грибов выражали в виде доли от общей ДНК, выделенной из зерновой муки (пг/нг общей ДНК). Нижний достоверный предел выявления содержания ДНК грибов в пробе общей ДНК был установлен на уровне 5×10-4 пг/нг общей ДНК.
Иммуноферментный анализ (ИФА)
Иммуноферментным методом анализировали со-держание двух микотоксинов – дезоксиниваленола (ДОН), образуемого F. graminearum и F. culmorum, и Т-2 токсина, образуемого F. sporotrichioides. Мико-токсины экстрагировали из 1 г муки, добавляя 5 мл водного раствора ацетонитрила (84:16, v/v), в условиях постоянного перемешивания на шейкере S-3M (ELMI, Латвия) при 300 об/мин в течение 14-16 часов. Анализ выполняли с помощью двух диагностических тест-систем для непрямого твердофазного конку-рентного ИФА: «Дезоксиниваленол-ИФА» и «Т-2 ток-син-ИФА» (ВНИИВСГЭ, Россия) – с нижним пределом чувствительности 20 и 4 мкг/кг соответственно. Для построения калибровочных кривых использовали стандарты микотоксинов в ацетонитриле с кон-центрацией 1 мкг/мл (ВНИИВСГЭ, Россия). ИФА вы-полняли на наборных полистироловых планшетах (Биомедикал, Россия) с последующим измерением оптической плотности растворов при длине волны 492 нм на фотометре LEDETECT 96 (Biomed, Австрия).
Статистический анализ
Все лабораторные анализы выполняли как минимум двукратно. Полученные результаты обрабатывали с помощью статистических программ Microsoft Excel 2010 и STATISTICA 10.0. Связь между количественными признаками оценивали с использованием линейного коэффициента корреляции Пирсона (r). Коэффициент вариации (V, %) рассчитывали как процентное отношение среднеквадратического отклонения к среднему арифметическому ряда показателей.
РЕЗУЛЬТАТЫ
Микологический анализ показал значительное при-сутствие грибов Alternaria и Fusarium во всех образцах зерна (Таблица 2). В отличие от пшеницы, в образцах зерна овса и ячменя выявлен B. sorokiniana. Кроме этих представителей микобиоты, из зерна были выделены изоляты других грибов: Microdochium Syd. & P.Syd., Aureobasidium Viala & G.Boyer, Epicoccum Link и Trichothecium roseum (Pers) Link.
| Культура | Сорт | Зараженность зерна грибами, % | ||||||
|---|---|---|---|---|---|---|---|---|
| Fusarium | Alternaria | B. sorokiniana | Epicoccum | Microdochium | Aureobasidium | T. roseum | ||
| Овес | Borrus | 66 | 42 | 4 | 4 | 0 | 3 | 0 |
| Всадник | 56 | 31 | 9 | 2 | 0 | 2 | 0 | |
| Ячмень | Инари | 84 | 18 | 10 | 0 | 0 | 7 | 0 |
| Криничный | 89 | 24 | 9 | 0 | 0 | 6 | 0 | |
| Пшеница | Сударыня | 56 | 26 | 0 | 2 | 9 | 0 | 2 |
| Тризо | 61 | 18 | 0 | 1 | 4 | 0 | 0 | |
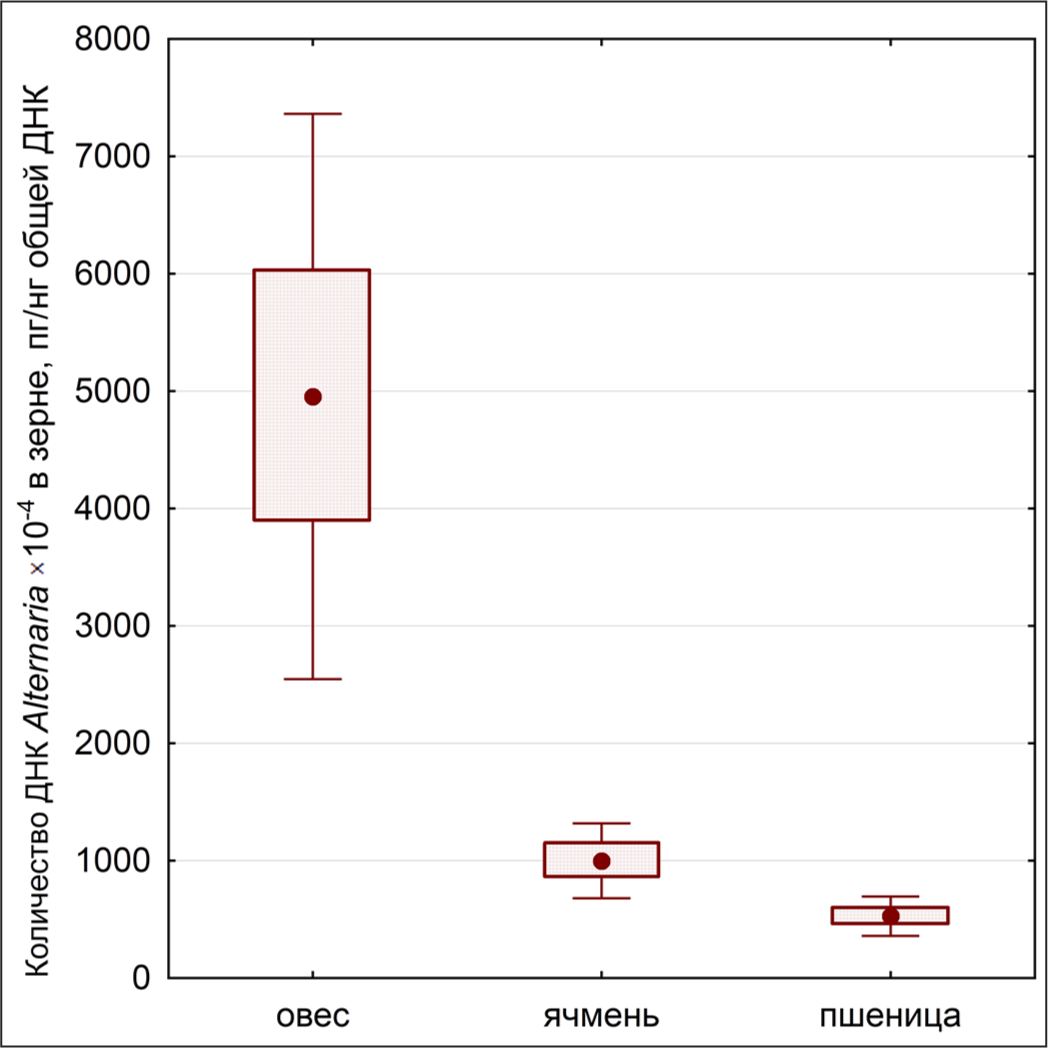
ДНК грибов Alternaria выявлена во всех анализированных образцах зерна. В среднем, зерно различных сортов овса содержало в 5 и 9 раз больше ДНК грибов Alternaria по сравнению с исследованными образцами сортов ячменя и пшеницы соответственно (Рис. 1). Наименьшее количество ДНК Alternaria определено в зерне пшеницы сорта Тризо (184×10-4 пг/нг), а максимальное количество Alternaria (11160×10-4 пг/нг общей ДНК) – в зерне овса сорта Озон.
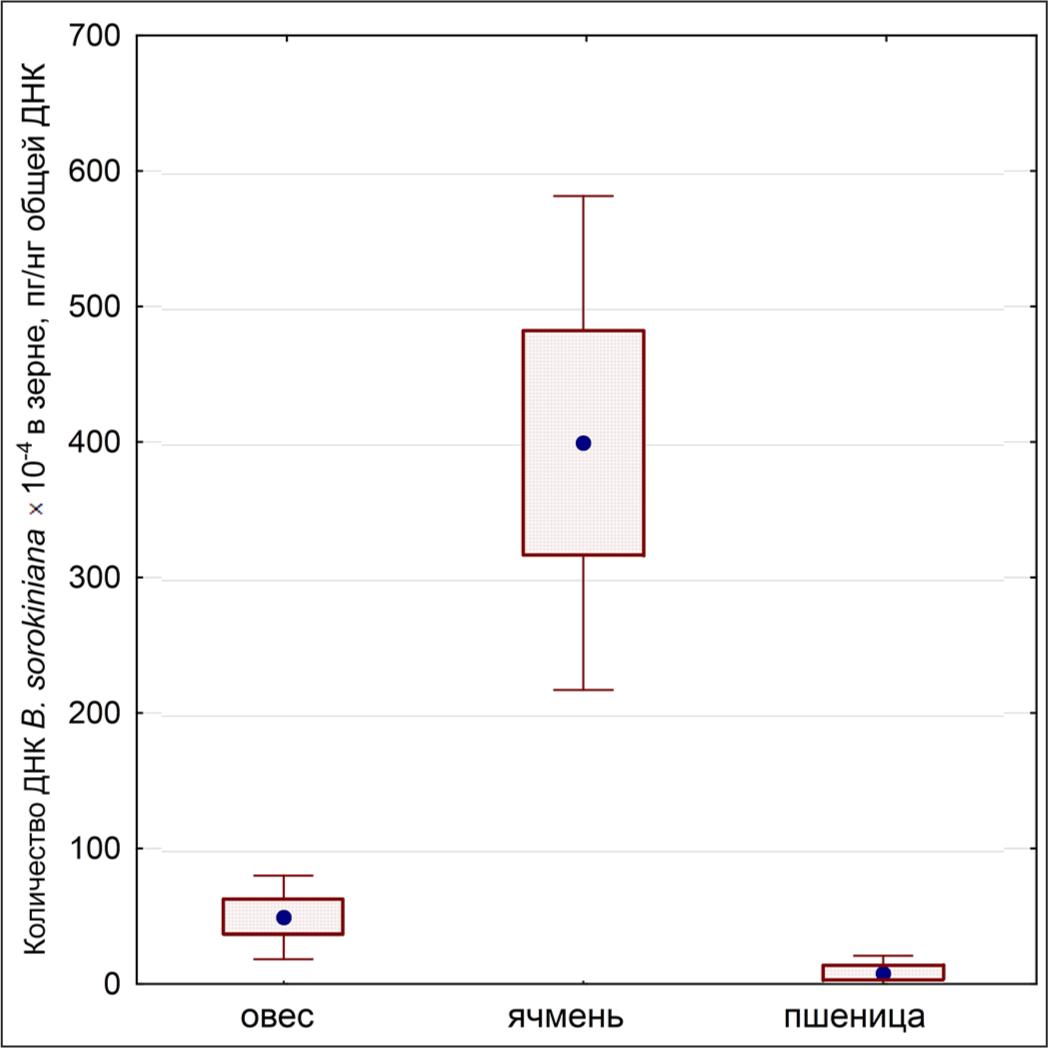
Впервые проведена оценка зараженности зерна российского происхождения грибом B. sorokiniana с помощью метода кПЦР (Рис. 2). Молекулярные праймеры, первоначально разработанные для качественной детекции ДНК этого патогена в зерне [10], успешно адаптированы нами для количественного анализа. ДНК B. sorokiniana выявлена в 100% образцов зерна ячменя и овса и только в 56% образцов пшеницы. В среднем, в образцах ячменя количество ДНК B. sorokiniana было существенно выше по сравнению с зерном овса и пшеницы. Максимум ДНК B. sorokiniana (648×10-4 пг/нг общей ДНК) выявлен в зерне ячменя сорта Олимпик.
Оценка содержания ДНК F. graminearum в зерне показала присутствие этого патогена во всех ана-лизированных образцах (Таблица 3). Максимальное количество ДНК F. graminearum выявлено в зерне ячменя сорта Фэст (1110×10-4 пг/нг). ДНК F. culmorum выявлена в 70% образцов овса и 100% образцов ячме-ня и пшеницы. Максимальное количество ДНК этого гриба – 90×10-4 пг/нг – обнаружено в зерне овса сорта Медведь. ДНК F. sporotrichioides, продуцирующего Т-2 токсин, не выявлена ни в одном из образцов зерна пшеницы, но обнаружена в 70% образцов овса и 50% – ячменя. В среднем, ДНК F. sporotrichioides выявлена в более низких количествах (до 47×10-4 пг/нг) по сравнению с другими видами грибов.
| Показатель | Количества ДНК грибов ×10-4, пг/нг общей ДНК, и микотоксинов, мкг/кг | |||||
|---|---|---|---|---|---|---|
| овес | ячмень | пшеница | ||||
| n+ а , % | среднее (диапазон) | n+, % | среднее (диапазон) | n+, % | среднее (диапазон) | |
| F. graminearum | 100 | 76 (14-261) | 100 | 170 (22-1110) | 100 | 203 (55-561) |
| F. culmorum | 70 | 21 (8-90) | 100 | 17 (9-43) | 100 | 22 (11-39) |
| F. sporotrichioides | 70 | 17 (5-47) | 50 | 6 (6-26) | 0 | 0 |
| ДОН | 100 | 357 (9-666) | 100 | 499 (77-2154) | 100 | 2318 (455-4471) |
| Т-2 токсин | 40 | 7 (5-12) | 67 | 22 (3-89) | 33 | 18 (2-38) |
n+ – количество образцов, в которых выявлен анализируемый показатель.
Микотоксин ДОН выявлен в 100% анализированных образцов зерна, с диапазоном количества от 77 до 4133 мкг/кг, в то время как T-2 токсин обнаружен только в 45% образцов в более низких количествах – от 2 до 89 мкг/кг (Таблица 3).
Сравнительный анализ загрязнения зерна трех культур микотоксинами показал, что в образцах пшеницы количество ДОН было достоверно выше, чем в образцах овса и ячменя. Содержание Т-2 токсина в образцах ячменя было выше по сравнению с образцами овса и пшеницы в 7 и 3 раза соответственно.
Минимальное количество ДОН выявлено в зерне ячменя сорта Ленинградский, а максимальное – в зерне пшеницы сорта Каликсо. При установленной высокой зараженности зерна продуцентами F. graminearum и F. culmorum ожидаемо выявлены образцы зерна, в которых среднее количество ДОН превышало предельно допустимую концентрацию (ПДК) этого микотоксина в зерне и зернопродуктах (700-1000 мкг/кг) [11]. Число образцов, загрязненных ДОН в количествах выше ПДК, составило 32% (сорта ячменя Московский 86, Фэст и все сорта пшеницы за исключением сорта Ленинградская 6). Те образцы зерна, в которых был выявлен Т-2 токсин, содержали его в количествах ниже установленной ПДК (100 мкг/кг) [11]. Максимальное количество этого микотоксина (89 мкг/кг) выявлено в зерне ячменя сорта Черио.
Корреляционный анализ экспериментальных данных выявил достоверную положительную связь (r=0.49, p <0.05) между количествами ДНК F. graminearum и ДОН в зерне. В то же время связи между количествами ДНК F. culmorum – другого продуцента ДОН – и этого микотоксина не установлено. Данный факт был также отмечен другими исследователями [12], показавшими, что F. culmorum продуцирует значительно меньшие количества ДОН по сравнению с F. graminearum [13].
Заслуживает внимания выявление высокой по-ложительной связи (r=0.72, p <0.01) между количе-ствами ДНК грибов Alternaria и F. sporotrichioides, что предполагает сходство условий для их развития на общем субстрате. Ранее мы уже отмечали, что при колонизации зерна овса между агрессивными видами Fusarium и относительно слабыми патогенами Alternaria возникают симбиотические взаимоотношения [14].
ОБСУЖДЕНИЕ
Грибы рода Alternaria встречаются в разнообразных растениях, но до настоящего времени их вредоносность является спорной. В наших исследованиях по-казана разница между зерновыми культурами по количеству биомассы Alternaria spp., однако внутри одного вида растения рассчитанный коэффициент вариации V содержания ДНК грибов был невысоким и сходным по величине (41–68%), что говорит об отсутствии дифференцированного взаимодействия в системе сорта и грибов рода Alternaria.
Гриб B. sorokiniana является вредоносным патогеном зерновых культур, в особенности ячменя. B. sorokiniana вызывает снижение всхожести зерна, пятнистость листьев, корневую гниль. Микологический анализ выявил зараженность этим патогеном только зерна овса и ячменя, но не обнаружил его в зерне анализированных сортов пшеницы. Полу-ченные методом кПЦР результаты подтверждают значительное содержание ДНК этого гриба в зерне ячменя, превышающее его содержание в зерне овса в 8 раз, а пшеницы – в 40 раз.
Мы провели анализ содержания ДНК грибов F. graminearum, F. culmorum и F. sporotrichioides, а также продуцируемых ими опасных микотоксинов. В образцах зерна количества ДНК F. sporotrichioides и, как следствие, образуемого им Т-2 токсина были низкими. Значительное загрязнение зерна ДОН, особенно в случае пшеницы, связано с высоким содержанием ДНК F. graminearum. Достоверная связь между содержанием ДНК гриба и микотоксина, продуцентом которого он является, позволяет использовать метод кПЦР для быстрой характеристики селекционного материала при создании устойчивых сортов, оценки эффективности фунгицидов и контроля качества получаемого урожая зерна или продукции на его основе. Количественная ПЦР является также удобным и объективным методом анализа в экспериментах, выявляющих взаимоотношения между растениями и представителями микобиоты. Быстрое обнаружение и оценка содержания патогенов позволяют объективно устанавливать в динамике воздействие раз-личных условий, а также определять эффективность мероприятий, направленных на снижение их вредо-носности.
ЗАКЛЮЧЕНИЕ
Высокая чувствительность метода количественного выявления ДНК грибов и относительная быстрота получения информации позволяют объективно определять содержание фитопатогенов в анализируемом материале. Адаптированный метод кПЦР позволил количественно оценить присутствие в урожае зерна пшеницы, овса и ячменя патогенных видов грибов F. graminearum, F. culmorum, F. sporotrichioides, B. sorokiniana, а также широко распространенных представителей рода Alternaria. Для всех анализированных образцов зерна показано высокое содержание грибов Alternaria, экологическая значимость которых до сих пор точно не известна. Гриб B. sorokiniana выявлен в зерне всех культур, однако отмечено значительное преобладание содержания ДНК этого патогена в зерне ячменя. Установленное высокое содержание ДНК F. graminearum в зерне всех культур является причиной значительного загрязнения зерна микотоксином ДОН.

