ВВЕДЕНИЕ
Грипп – одно из наиболее распространенных инфекционных заболеваний. В России ежегодно регистрируется около 50 млн. случаев инфекционных заболеваний и около 95% из них приходится на острые респираторные вирусные инфекции (ОРВИ), включая грипп. При этом по данным Федерального центра по гриппу и ОРЗ, заболеваемость среди детей в 7–10 раз превышает показатели, регистрируемые в группе взрослого населения. В период гриппозной пандемии показатели заболеваемости и смертности всего населения существенно возрастают по сравнению с ежегодными эпидемиями [1].
В соответствии с глобальной концепцией, изложенной в директивных документах ВОЗ, реальность возникновения новых возбудителей, включая потенциально пандемические шифт-варианты вируса гриппа, определяет настоятельную необходимость дальнейшего развития служб надзора за респираторными вирусными инфекциями в целях раннего распознавания предстоящих пандемических событий и идентификации новых вирусов гриппа [2].
Поскольку ОРВИ разной этиологии зачастую имеют сходную клиническую симптоматику, особенно на начальных этапах, особую значимость приобретает совершенствование и развитие современных методов лабораторной дифференциальной диагностики. Ранняя идентификация гриппозной инфекции позволяет назначить этиотропную терапию в самом начале заболевания, предупредить развитие вторичных инфекций разной этиологии и ограничить применение антибиотиков. Своевременная расшифровка природы эпидемических вспышек необходима для определения тактики проведения противоэпидемических мероприятий и структуры экстренных превентивных мер в очагах заболеваний. В этой связи особую значимость приобретает совершенствование и развитие современных методов лабораторной диагностики гриппа и других ОРВИ.
Наиболее простым и доступным лабораторным методом идентификации вновь выделенных вирусов гриппа остается реакция торможения гемагглютинации (РТГА) с использованием субтипспецифичных иммунных сывороток животных. Метод позволяет визуально учитывать результаты взаимодействия антиген-антитело без использования какого-либо оборудования. Однако длительная аккумуляция эволюционных мутаций в молекуле гемагглютинина (НА) циркулирующих в человеческой популяции вирусов гриппа А(H1N1) и, особенно, A(H3N2) затронула и рецептор-связывающий сайт HA, что привело к снижению его аффинности к рецепторам эритроцитов различной видовой принадлежности [3-6]. В результате возникли трудности в идентификации подтипов (серотипировании) некоторых современных штаммов с использованием общепринятого метода РТГА.
Одним из альтернативных методов выделения и анализа новых патогенов считается микрокульту-ральный иммуноферментный метод cell-ELISA, основанный на оценке репродукции вируса в инфицированной культуре клеток c использованием на стадии детекции высокоспецифичных моноклональных антител (mAb), взаимодействующих с вирусными белками. Метод cell-ELISA, с использованием mAb, специфичных к NP-белку вируса гриппа, рекомендован ВОЗ для оценки активности вируснейтрализующих антител в реакции микронейтрализации [7]. Этот метод с успехом используют также для детекции штаммов вируса гриппа, слабо реагирующих в РГА [8].
Поскольку NP-белок высоко консервативен, cell-ELISA с применением NP-специфичных mAb позволяет детектировать вирусы гриппа А любого подтипа, но при этом не дискриминирует его субтип, т.е. не подходит для серотипирования.
Целью проведенной работы была разработка чувствительного варианта cell-ELISA для субтипо-вой дифференциации современных вирусов гриппа А(Н1N1)pdm09 и А(Н3N2), циркулирующих в челове-ческой популяции.
МАТЕРИАЛЫ И МЕТОДЫ
Выделение вирусов гриппа из клинических образцов
В работе использованы штаммы вирусов гриппа А, выделенные из клинических материалов, полученных от больных гриппом и ОРВИ в различных городах России в период эпидсезона 2014 года.
Сбор клинических образцов и выделение из них вирусов гриппа А в культуре клеток MDCK или развивающихся куриных эмбрионах проводили согласно Методическим рекомендациям [9]. Идентификацию выделенных штаммов вируса гриппа А проводили с использованием РТГА и полимеразноцепной реакции (ПЦР).
Реакция гемагглютинации (РГА) и торможения гемагглютинации (РТГА)
РГА и РТГА ставили общепринятым методом в соот-ветствии с Практическими рекомендациями [10]. Для увеличения чувствительности методов использовали эритроциты человека (Rh+ группы 0).
ПЦР
Постановку ПЦР осуществляли с использованием наборов реагентов «АмплиСенс» («ИнтерЛабСервис», г. Москва) в соответствии с Инструкцией по применению системы. Выделение РНК из образцов проводили с использованием набора «АмплиСенсРИБопреп», для проведения обратной транскрипции вирусной РНК использовали наборы «АмплиСенсReverta». Для проведения ПЦР в реальном времени использовали системы “АмплиСенс® Influenzavirus A/B-FL” (анализ РНК вирусов гриппа типов А и В), “АмплиСенс® Influenzavirus A type FL” (субтипирование вирусов гриппа H1/H3) и “АмплиСенс® Influenzavirus A/H1–swine-FL”(выявление вируса гриппа А(H1N1)pdm09).
Получение моноклональных антител (mAb)
Панели mAb к вирусам гриппа А(Н3N2) и А(H1N1) pdm09 были получены в лаборатории биотехнологии диагностических препаратов НИИ гриппа по методу [11] c некоторыми модификациями. Мышей линии BALB/c или гибридов F1(BALB/c Х SJL/J) иммунизи-ровали путем внутрибрюшинного введения вирусов, очищенных ультрацентрифугированием в градиенте плотности сахарозы. Через несколько недель мышей бустировали очищенной фракцией поверхностных гликопротеинов того же вируса. Через 3 суток после бустер-иммунизации проводили гибридизацию спленоцитов иммунизированных мышей с клетками мышиной миеломы линии X63Ag8.653 в присутствии 50% ПЭГ-2000. Клонирование гибридных клеток проводили методом предельных разведений. При первичном анализе клонов использовали традиционный метод ИФА: тестируемую культуральную жидкость вносили в лунки планшетов, сенсибилизированных вируссодержащим материалом, с последующей детекцией прореагировавших mAb пероксидазным конъюгатом к IgG мыши («Sigma», США). Гибридные клоны с заданным спектром реагирования реклони-ровали на селективной среде НАТ. Стабильные кло-ны-продуценты mAb использовали для получения асцитов.
Мышам линии BALB/c или F1 (BALB/c Х SJL/J), предварительно праймированным пристаном (0.5 мл/мышь), внутрибрюшинно вводили гибридные клетки в количестве (3–5)×106 клеток/мышь. Спустя 2–3 не-дели асцитную жидкость собирали. Исследования выполняли согласно «Пpавилам пpоведения pабот с иcпользованием экспеpиментальных животных» (приказ № 266 МЗ РФ от 19.06.2003).
Микрокультуральный ИФА для оценки репродукции вирусов гриппа А в культуре клеток
Репродукцию вируса в клетках оценивали по со-держанию внутриклеточного НА. Для этого в лунки 96-луночных планшетов для культуральных работ («NUNC», Дания) с монослойными культурами клеток MDCK вносили 100 мкл исследуемого вируссодержа-щего материала и культивировали в СО2-термостате при 37°C. В качестве культуральной среды использо-вали alpha-MEM (OOO «БиолоТ», Санкт-Петербург) с 0.2% бычьего сывороточного альбумина (фракция V) («Sigma», США); 0.05% аргинина («Sigma», США) и 2 мкг/мл TPCK-трипсина («Sigma», США). Через 48– 96 ч инкубации (после появления цитопатического действия или при его отсутствии) из лунок удаляли культуральную среду, планшеты отмывали 0.01 М фосфатносолевым буфером, рН 7,2 (ФСБ) и клетки фиксировали 80% холодным ацетоном в течение 20 мин. После промывки ФСБ на монослой наносили блокирующий раствор (5% обезжиренное молоко в ФСБ, ФСБ-М), и инкубировали при 37°C в течение 1 ч с последующим внесением 100 мкл/лунку субти-поспецифичных mAb к НА вируса гриппа А(H1N1) pdm09 или A(H3N2) в концентрации 5–10 мкг/мл в ФСБ-М. После 2-ч инкубации при 37° С и удаления несвязавшихся первичных антител в лунки добавляли пероксидазный конъюгат антител к IgG мыши («Sigma», США) в ФСБ-М (в разведении 1/10 000); планшеты инкубировали в течение 1 ч при 37°С, отмывали и добавляли раствор субстрата, содержащий 0.1 мг/мл 3,3’,5,5’-тетраметилбензидина (ТМБ) и 0.02% Н2О2 в ацетат-цитратном буфере, рН 5.0. После остановки реакции раствором 2 N H2SO4 измеряли оптическую плотность на спекторофотоме-тре Anthos-2010 (Австрия) при длине волны 450 нм (ОD450). Положительными по репродукции вируса считали пробы, в которых значения ОD450 в два и бо-лее раз превышали таковые в лунках с незараженной культурой клеток (негативный контроль).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При отработке метода cell-ELISA использованы штаммы вирусов гриппа A(H1N1)pdm09, выделенные из клинических образцов в эпидсезон 2014 года (1–3 пассажа). Вирусы А(H3N2) изолировали в культуре клеток MDCK, а вирусыA(H1N1)pdm09 – в развивающихся куриных эмбрионах. Наличие вируса гриппа во всех образцах подтверждали с помощью ПЦР и РГА с использованием эритроцитов человека. Титры гемагглютинации вирусов варьировали от 1/4 до 1/64.
Для обнаружения вирусов, реплицирующихся в инфицированных культурах клеток MDCK, сначала проанализировали клетки, инфицированные эталонными штаммами вирусов гриппа А, и выбрали из панели полученных mAb три: #1 и #2, наиболее эффективно взаимодействующие с вирусами гриппа А/Техас/50/2012 и А/Швейцария/9715293/2013 (H3N2), а также #4, специфически связывающееся с вирусом гриппа A(H1N1)pdm09 (штамм А/Калифорния/07/2009). При предварительном скрининге выбранных антител с использованием ряда иммунологических методов (иммуноблоттинга, ИФА, РТГА) показано, что mAb #1, #2 и #4 направлены к НА1 субъединице и являются строго субтипспецифичными.
В дополнение к субтиповой дифференциации, наличие в культуре репродуцирующихся вирусов было доказано в cell-ELISA при использовании типоспецифичных антител, mAb #3, взаимодействующих с NPбелком вирусов гриппа А.
Результаты анализа изолятов вирусов гриппа А в cell-ELISA представлены на Рис. 1, 2. Для mAb #1, #2 и #4 не было зарегистрировано перекрестной реакции с клетками, инфицированными вирусами гетерологичных субтипов. С использованием mAb #1, #2 или #4 в концентрации 10–15 мкг/мл специфично выявляли синтезированный в зараженных клетках НА вирусов гриппа А(H3N2) или A(H1N1)pdm09, соответственно.
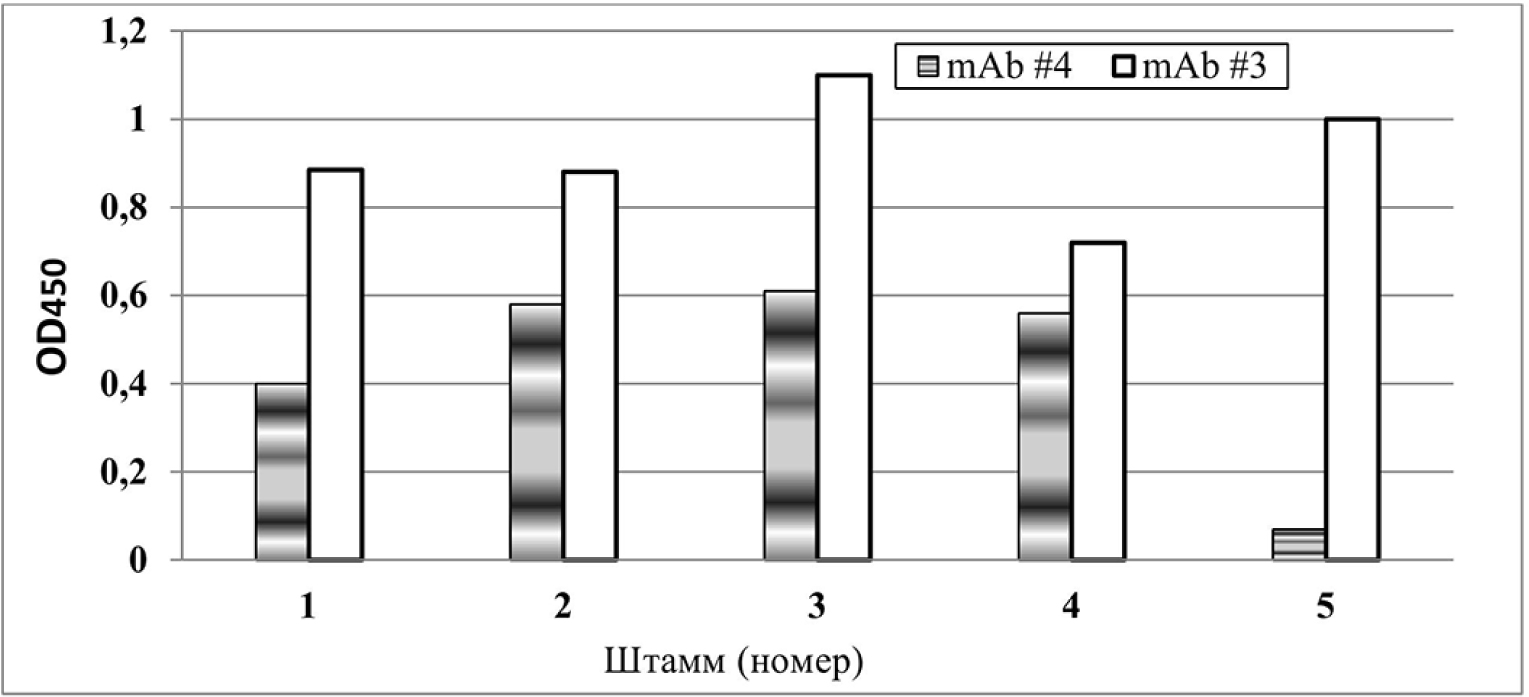
Представленные результаты получены методом cell-ELISA на следующих штаммах А(H1N1)pdm09:
1 – А/Санкт-Петербург/1/2014
2 – А/Санкт-Петербург/16/2014
3 – А/Санкт-Петербург/46/2014
4 – А/Калифорния/07/2009
Вирус гриппа А/Техас/50/2012 (H3N2) (5) использован как контроль специфичности антитела #4, направленного к субъединице HA1 вируса гриппа A(H1N1)pmd09. Универсальное антитело #3, специфичное к белку NP вирусов гриппа A любых подтипов, использовано как позитивный контроль репликации.
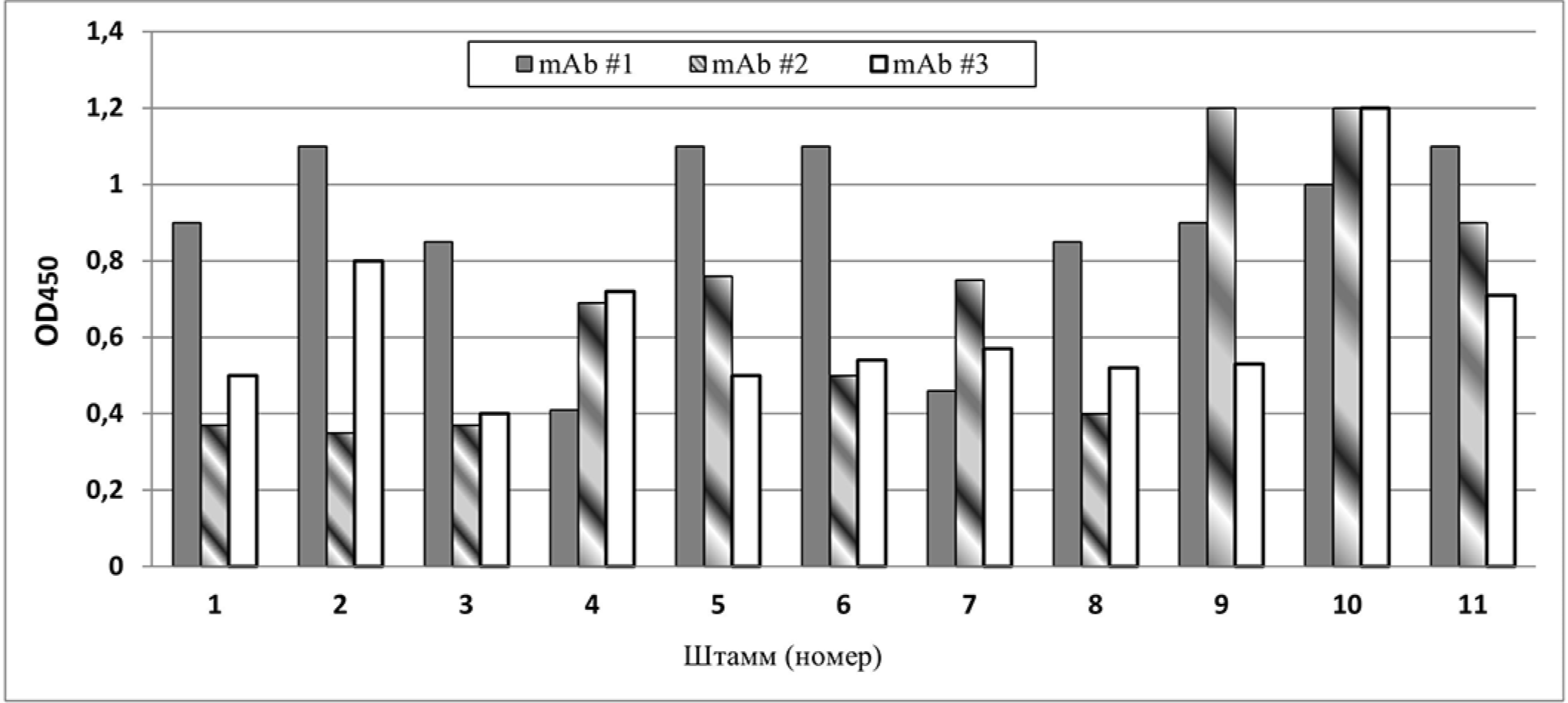
Антитела #1 и #2 связываются c HA1 субъединицей вирусов гриппа H3N2, а #3 с белком NP вирусов гриппа А.
Штаммы вируса гриппа А(Н3N2):
1–A/Астрахань/23/2014
2–A/Астрахань/24/2014
3–A/Астрахань/25/2014
4– А/Астрахань/26/2014
5– А/Чита/261/2014
6– А/Чита/258/2014
7– А/Чита/257/2014
8– А/Санкт-Петербург/80/2014
9–A/Москва/252/2014
10– А/Техас/50/2012
11– А/Швейцария/9715293/2013
Таким образом, микрокультуральный вариант ИФА (cell-ELISA) на основе моноклональных антител, специфически взаимодействующих с вирусным HA, может быть использован в качестве дифференциального метода диагностики современных штаммов вируса гриппа А в процессе их репродукции в клеточной культуре.

