ВВЕДЕНИЕ
Анализ структуры заболеваемости и смертности от гриппа в мировой практике основан на изучении возрастного распределения и выявлении групп риска [1–6]. Вместе с тем очевидно, что заболеваемость и смертность в существенной степени зависят от генетических особенностей отдельных популяций и этнических групп. С одной стороны, установлена прямая связь осложненного течения гриппа c гаплотипом HLA (Human Leucocyte Antigens), с другой – анализ полиморфизма ряда генов, определяющих уровень противовирусной защиты, подтверждает, что вклад отдельных мутаций и однонуклеотидных полиморфизмов (Single-Nucleotide Polymorphism; SNP) в заболеваемость и смертность от гриппа существенно выше, чем считалось ранее [7–12]. Масштабные исследования в области генетики популяций и чувствительности к гриппу свидетельствуют о том, что противоэпидемические мероприятия в различных регионах страны необходимо планировать в соответствии с генетическими особенностями населения. Также очевидно, что при разработке противогриппозных вакцин необходимо учитывать возможность их «генетической» ориентации на крупные группы населения и вероятность слабой реакции – вплоть до ее отсутствия – на вакцинацию у людей с определенными гаплотипами HLA [11, 12]. Основываясь на данных анализа генетических полиморфизмов, можно говорить о том, что в терапии гриппа – в условиях массовой заболеваемости, характерной для пандемий, – необходимо учитывать возможный характер осложненного течения заболевания, связанного с дефектом того или иного звена иммунитета и противовирусной защиты. Понимание генетических основ патологии инфекционных заболеваний, включая грипп, может существенно изменить как практику вакцинации, так и основы терапии.
В связи с этим необходимо систематизировать доступную информацию по структуре генов и генетических маркеров, характерных для случаев неадекватных или патологических реакций при заболевании гриппом и сопутствующими инфекциями.
Ниже представлены перечень и характеристика генов, SNP в которых ассоциируется с повышением чувствительности к заражению гриппом или тяжелым течением заболевания [9, 13, 14].
Роль полиморфизма гена интерферониндуцируемого трансмембранного белка 3 (IFITM3) в инфекционной патологии
Ген (IFITM3). Одним из важных открытий за период, прошедший со времени последней пандемии, мож-но считать выявление полиморфизма в гене IFITM3 в когортах пациентов, у которых пандемический вирус гриппа A(H1N1)pdm09 вызывал тяжелое течение заболевания, в ряде случаев с фатальными осложнениями (Рис.1) [9, 13–21].
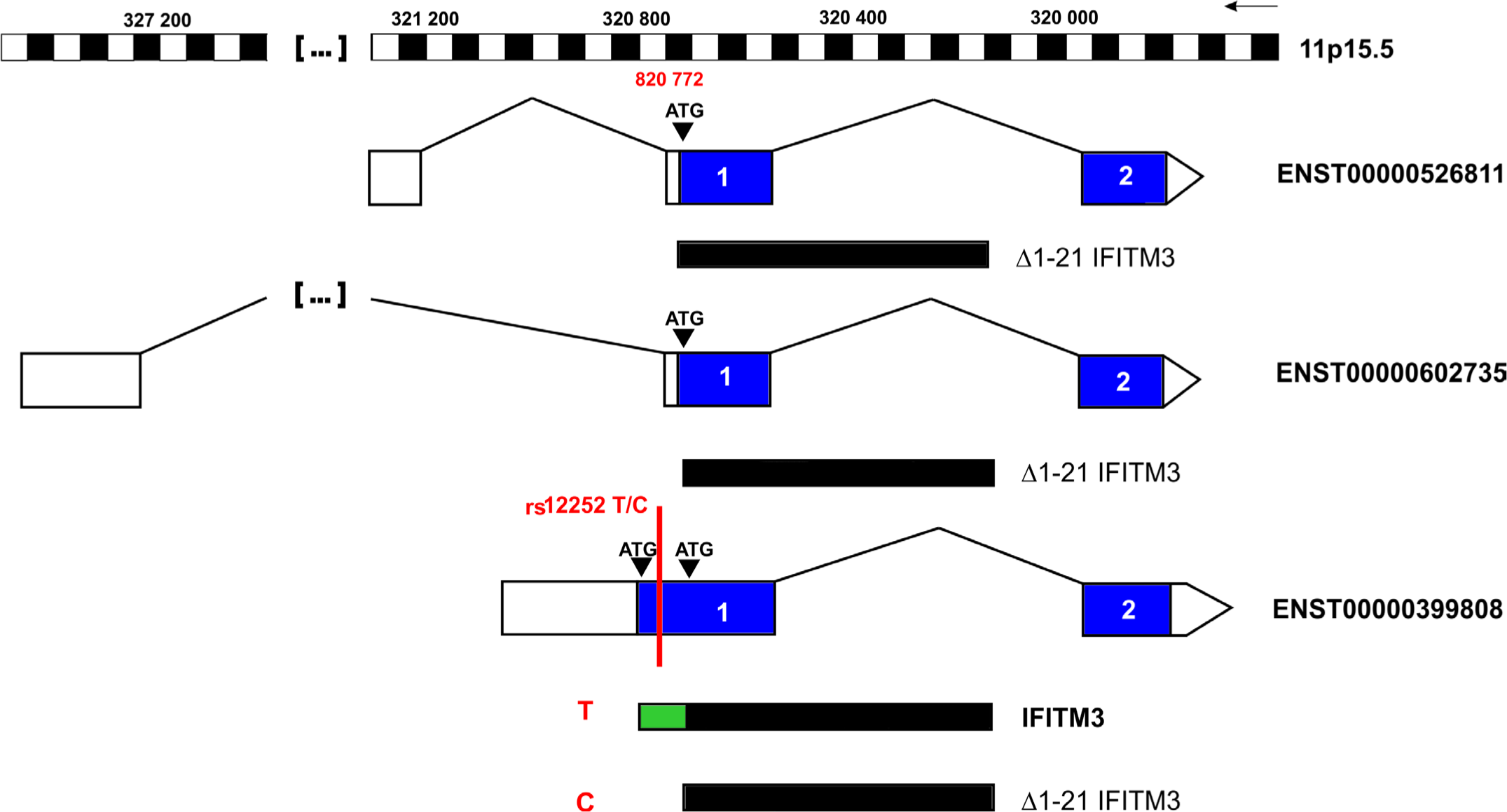
Мутация, приводящая к образованию альтернативного сайта сплайсинга в экзоне 1 обозначена вертикальной красной чертой (однонуклеотидный полиморфизм rs12252 Т/С). Черными треугольниками отмечены старт-кодоны, синим цветом – белок-кодирующие экзоны гена IFITM3, зеленым цветом – фрагмент 1-21 белка IFITM3 [26].
Ген IFITM3 входит в семейство генов, активность которых индуцируется интерферонами (IFN) I типа. Белок IFITM3 относится к трансмембранным белкам и включает два трансмембранных домена. Его функциональная активность связана с устойчивостью к штаммам A(H1N1)pdm09 и многим другим инфекциям, включая лихорадку Денге и геморрагическую лихорадку Западного Нила [13]. Белок IFITM3 существует в различных изоформах, и одна из них, достаточно распространенная, лишена N-концевого домена (Рис.2) [18–21]. Анализ этого явления привел к идентификации мутации по сайту сплайсинга, которая и определяет повышенную чувствительность к пандемическому гриппу [19, 20].
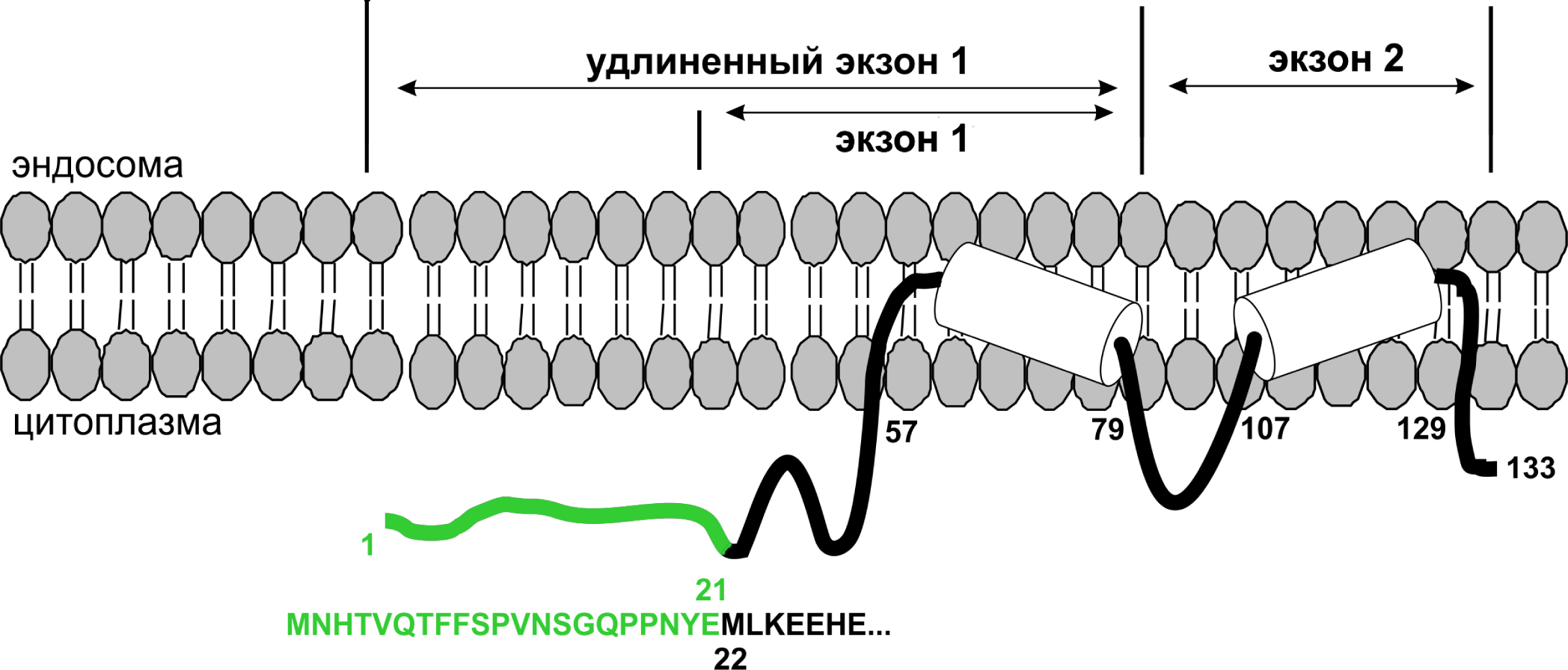
Зеленым цветом выделена N-концевая последовательность 1-MNHTVQTFFSPVNSGQPPNYE-21, отсутствующая в укороченной форме белка.
При анализе механизма действия IFITM3 выявлено, что этот белок блокирует инфицирование клеток (проникновение вируса в клетки) на уровне эндоцитоза вирусных частиц [22]. Позднее установлена его роль в подавлении инфекций, вызванных такими вирусами, как Эбола, вирус иммунодефицита человека I типа (ВИЧ-1), гепатит С, лихорадка Денге [13]. Также показано, что IFITM3 подавляет зависимый от S-белка эндоцитоз коронавируса ближневосточного респираторного синдрома (Middle East Respiratory Syndrome; MERS) [23], тем самым препятствуя проникновению генетического материала вируса в клетку.
Широкий спектр противовирусной активности белка IFITM3 объясняется тем, что он оказывает сильнейшее влияние на стабильность комплекса АТФазы вакуолей (в-АТФаза) и эндосом. В эндоцитозе вирусов важная роль принадлежит взаимодействию в-АТФазы с эндосомами, что приводит к изменению локализации клатрина и снижению рН [24]. Этот процесс играет ключевую роль в инфицировании клеток, поэтому особенно привлекателен в качестве терапевтической мишени. Установлено, что классические ингибиторы клатрина и в-АТФазы – эффективные ингибиторы репродукции вирусов и относятся к препаратам широкого спектра действия. Оказалось, что в этот «список» входит Арбидол [25]. Таким образом, у Арбидола выявили еще один механизм действия, который, по-видимому, и обусловливает его проти-вовирусную активность к широкому спектру вирусов. Однако механизм противовирусной защиты не может быть полным обоснованием механизмов интер-ференции IFITM3 с вирусами на уровне клатринового пути интернализации вирусных частиц на ранних этапах инфекции.
В ходе экспрессии гена IFITM3 могут образовываться два разных транскрипта: полный и его усеченный вариант, который кодирует последовательность белка, лишенную N-концевого фрагмента протяженностью в 21 аминокислотный остаток [21].
В общем случае, белок IFITM3 – это фактор ре-стрикции вирусной репродукции, действующий через формирование клеточной резистентности к вирусам различных семейств. Но детальные механизмы формирования противовирусной защиты в клетках, несмотря на открытие белка IFITM3, остаются неизвестными. В ряде работ [18–20] показано, что у мышей с нокаутированным геном IFITM3 течение гриппозной инфекции протекает тяжелее, чем у животных с диким типом этого гена. В человеческой популяции известна мутация по этому гену – замена Т на С в сайте сплайсинга I интрона [18].
Исследована связь этой мутации в Европейской по-пуляции с течением гриппозной инфекции, вызванной вирусом A(H1N1)pdm09, и частотой госпитализации, что считалось критерием осложненного развития инфекции [19]. У пациентов, госпитализированных с осложненным гриппом и тяжелым течением заболевания, выявлена повышенная частота гомозиготности по редкому аллелю С гена IFITM3. Частота SNP rs12252-C у тяжелых пациентов составляла 5.3% по сравнению с 0.3% для Европейской популяции. Инте-ресно, что в популяциях Китая частота встречаемости SNP rs12252-C оказалась существенно выше. Так если в среднем частота генотипа СС составляла около 25%, то среди пациентов из Китая с тяжелыми формами гриппа встречаемость генотипа СС доходила до 69% (Рис. 3).
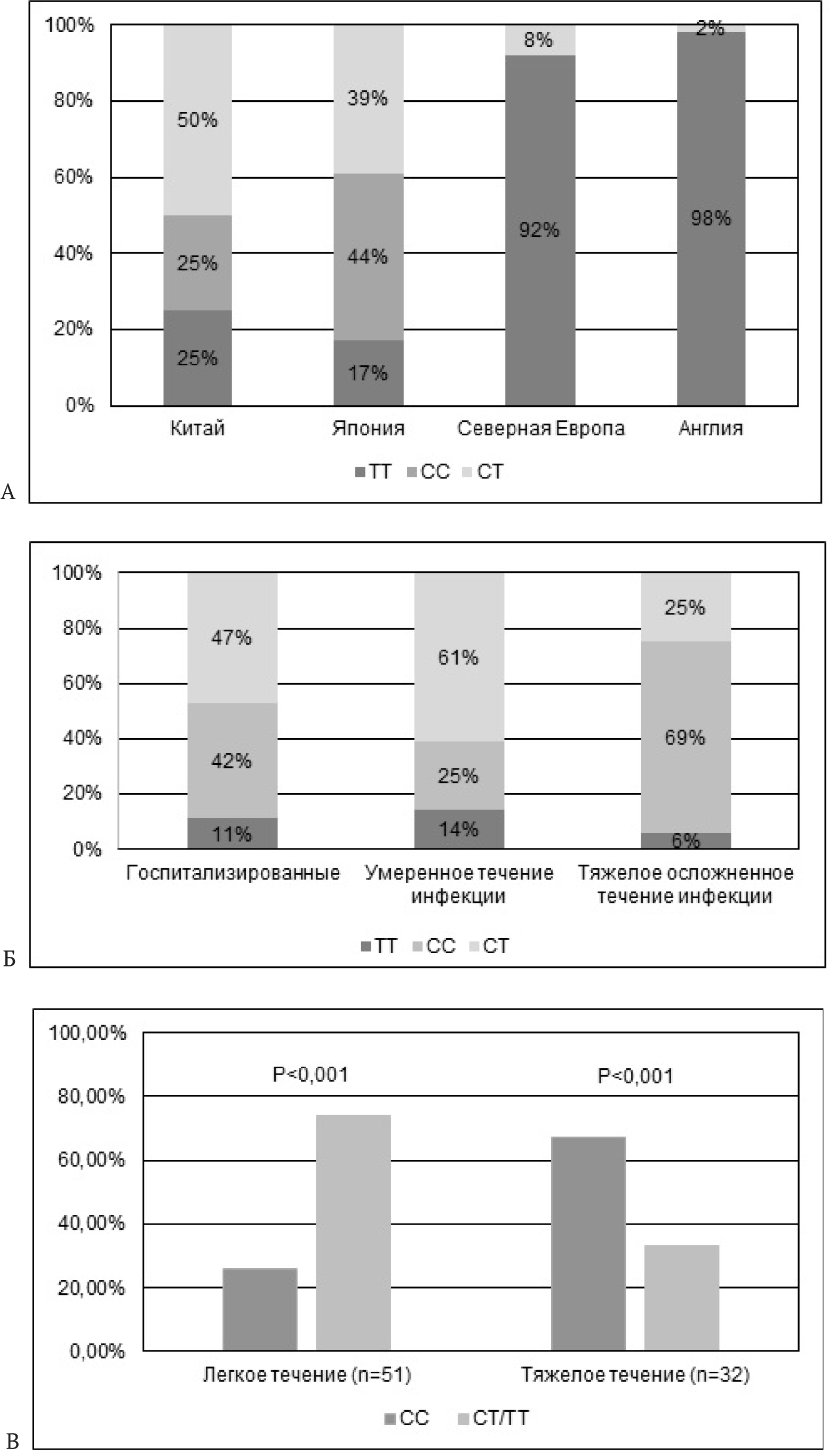
А – сравнение генотипов в популяциях Китая, Японии, Северной Европы и Англии;
Б – категории больных: 1 – госпитализированные, 2 – грипп средней тяжести, 3 – осложненное тяжелое течение гриппа;
В – частота встречаемости аллелей у больных вирусом A(H1N1)pdm09.
Приведенные результаты по частоте аллелей гена IFITM3 получены авторами при статистической обработке данных по 1 000 геномов [19]. Частота аллелей сильно варьировала в различных популяциях. Однако среди популяции Хан, происходящей из Южной провинции и населяющей Восток, Юг и центральный Китай, частота СС генотипа rs12252 достигала 69%. В результате детального анализа генетической структуры популяции и заболеваемости (смертности) гриппом авторы приходят к выводу, что высокая частота генотипа СС вносит вклад в эпидемиологию гриппа на территории Китая. Действительно, именно на территории Китая регистрируется высокая частота масштабных вспышек гриппа, которые нередко приводят к пандемиям.
В связи с обнаруженной корреляцией между генотипом IFITM3 rs12252 и клинической картиной гриппозной инфекции представляло интерес изучение отдельных компонентов «цитокинового штор-ма» у пациентов с вариантным геном IFITM3 [21]. Эти исследования проведены на пациентах, инфицированных циркулирующим на современном этапе патогенным штаммом вируса гриппа А(H7N9). Проанализирована экспрессия следующих маркеров «цитокинового шторма»: MPC-1 (Monocyte Chemoattractant Protein-1), IL-1β (Interleukin-1β), IL-6, IL-8, IL-10, ТNF-α (Tumor Necrosis Factor), IFN-γ и С-реактивный белок [27]. Авторы исследовали со-держание этих белков в периферической крови. В ре-зультате установлено, что у пациентов с генотипом СС уровень синтеза и секреции белка MPC-1 существенно выше по сравнению с пациентами с генотипами СТ или ТТ (Рис. 3). И тяжесть заболевания напрямую коррелировала с этими показателями – генотипом СС и чрезмерным неспецифическим иммунным ответом. Более того, авторами проведено исследование цитокинов (MIP-1α, MIP-1β, IL-1β, IL-6 и IL-8) в легких погибших пациентов. Оказалось, что содержание некоторых провоспалительных цитокинов было в 100–1 000 раз выше в легких по сравнению с периферической кровью. Таким образом, мутация гена IFITM3 rs12252 способствует развитию «цитокинового шторма».
В завершение рассмотрения роли полиморфизма гена IFITM3 в инфекционной патологии следует отметить, что SNP rs12252 вносит вклад в развитие болезни Кавасаки – раннего детского васкулита [15]. Эта патология также характерна для отдельных групп населения Юго-Восточной Азии и может приводить к такому тяжелому осложнению, как аневризма аорты [28]. Следует заметить, что гриппозная инфекция провоцирует васкулиты, в том числе цереброваскулиты, а это позволяет предполагать влияние гриппозной инфекции на развитие сердечно-сосудистой патологии.
Полиморфизм генов, вносящих дополнительный вклад в тяжелое течение гриппозной инфекции
Исследование полиморфизма генов для понимания предрасположенности к инфекционным заболеваниям и их тяжелому течению имеет фундаментальное значение для педиатрической практики и глобальных эпидемических процессов [9, 14, 17]. Репертуар генов, в той или иной степени определяющий развитие осложнений гриппа, с годами существенно расширяется [9, 17]. В таблице 1 представлен перечень этих генов и их вероятный вклад в нарушение тех или иных функций в эрадикации гриппозной и других вирусных инфекций.
| Ген | Функция кодируемого белка | Дефект | Ссылка |
|---|---|---|---|
| IFITM3 | Фактор противовирусной защиты на уровне эндосом | Дефект внутриклеточной противовирусной защиты на раннем этапе инфекции (эндосомы) | [18, 19, 21, 25] |
| SP-B | Сурфактантный белок В – легочный сурфактант | Защита пневмоцитов, стабильность альвеол, транспорт кислорода и клиренс вирусов и бактерий | [29, 30] |
| FCGR2A | Fc-рецептор – фактор клиренса инфекционного вируса | Дефект клиренса вируса | [31, 32] |
| C1QBP | Фактор системы комплемента | Дефект системы комплемента и комплемент – зависимого цитолиза инфицированных клеток | [8, 9, 33] |
| DAF/CD55 | Фактор ускорения распада комплемента, антиген системы групп крови Кромера | Дефект врожденных механизмов защиты легких от комплемент-опосредованного поражения при гриппозной инфекции | [34] |
| MBL2 | Маннозосвязывающий клеточный лектин | Дефект регуляции врожденного иммунитета | [35] |
| SOCS4 | Супрессор цитокин-зависимых сигнальных систем | Дефект контроля синтеза и активности цитокинов (возможно развитие «цитокинового шторма») | [27, 36] |
| SECISBP2 | Комплекс Se-зависимых ферментов | Дефект антиоксидантной системы | [37] |
Белки легочного сурфактанта несут важнейшие функции не только в обеспечении стабильности транспорта кислорода, но и в антибактериальной и противовирусной защите. Многолетние клинические наблюдения показали, что полиморфизм генов, кодирующих сурфактантные белки и, в частности белок В (SP-B), играют ключевую роль в чувстви-тельности к таким инфекциям, как грипп [29]. Также установлено, что полиморфизм гена SP-B связан с тяжелым течением инфекции, вызванной респираторно-синцитиальным вирусом [30].
Хорошо известна роль факторов системы комплемента в бактериальных и вирусных инфекциях. В этом отношении особого внимания заслуживают данные о роли полиморфизма в гене C1QBP (Complement Component 1, Q subcomponent Binding Protein) в осложненном течении гриппа [8, 33]. Ген C1QBP кодирует белок C1QBP, который в зрелом виде представляет собой гомотример. Особенность строения гомотримера C1QBP состоит в том, что он имеет ассиметричное распределение заряда на поверхности молекулы. Белок взаимодействует с широким набором молекул, вовлеченных в регуляцию иммунной системы: CDK13 [38] , HRK [39], VTN [40], NFYB [41], FOXC1 [42], DDX21, DDX50, NCL [43], SRSF1, SRSF9 [44], CDKN2A [45] — и другими белками, включая СD93 [46]. Функция C1QBP состоит в антитело-зависимом цитолизе инфицированных клеток при участии комплемента и активации фагоцитоза. Белок накапливается в митохондриях в процессе вирусной инфекции и ингибирует зависимую от RLR (RIG-I-like receptors) передачу сигнала путем взаимодействия с противовирусным белком MAVS (Mitochondrial AntiViral-Signaling protein). Белок C1QBP вовлечен в активацию коагуляционного каскада крови [47]. Действие C1QBP носит плейотропный характер и зависит от стадии инфекции.
CD55 (Complement Decay-Accelerating Factor; DAF) – фактор ускорения распада комплемента, антиген системы групп крови Кромера. DAF/CD55 выполняет противовоспалительные функции, защищая клетки от повреждения со стороны системы комплемента, а также контролируя миграцию лейкоцитов в очаг воспаления [47]. DAF/CD55 экспрессирован в эндотелии сосудов, мононуклеарах периферической крови, а также эпителиальных клетках (в том числе в эпителии легких и эндометрии) [48]. CD55 подавляет активацию компонентов C3 и C5 системы комплемента [49]. Значительный уровень экспрессии CD55 в респираторном эпителии подчеркивает важность защиты легких от повреждения в результате избыточной активации системы комплемента. Интересно отметить, что уровень экспрессии CD55 регулируется прогестероном и эстрогеном [50].
SNP в промоторе гена CD55 (rs2564978 генотип Т/T) ассоциирован с более тяжелым течением гриппа, вызванного вирусом гриппа A(H1N1)pdm09 [34]. В экспериментах in vitro установлено, что заражение клеток вирусом гриппа A(H1N1)pdm09 вызывает усиление экспрессии белка CD55. У пациентов с генотипом T/T rs2564978 значительно снижен уровень CD55 на поверхности мононуклеаров периферической крови по сравнению с пациентами с генотипами C/C и C/T [51].
Активация системы комплемента вносит существенный вклад в поражение легочной ткани при гриппозной инфекции. В легких мышей, зараженных вирусами гриппа А(H5N1), обнаружен высокий уровень C3, C5b-9, MBL, а введение антагониста C3aR значительно снижает уровень воспаления в легочной ткани [52].
Мутация в промоторе гена CD55, по-видимому, приводящая к снижению его экспрессии, нарушает врожденные механизмы защиты легких от компле-мент-опосредованного поражения при гриппозной инфекции, повышая риск тяжелого течения болезни и летального исхода.
В рамках рассмотрения проблемы полиморфизма генов человека и их связи с тяжелым течением грип-позной инфекции со всей очевидностью на передний план выходит проблема последствий неадекватной реакции врожденного иммунитета на инфекцию. Из-вестно, что важную роль в патогенезе осложненного гриппа играет активация транскрипции генов, коди-рующих провоспалительные цитокины [21].
В связи с этим особый интерес представляет система генетического контроля реакции врожденного иммунитета на гриппозную инфекцию и функции генов, вовлеченных в негативную регуляцию экспрессии генов, кодирующих провоспалительные цитокины. Ген SOCS4 (Suppressor Of Cytokine Signaling 4) занимает в иерархии генетического контроля активации синтеза провоспалительных цитокинов одно из ключевых положений [36].
Естественен интерес к генетическому контролю этих процессов со стороны природных факторов. Недавно установлено, что гены семейства SOCS играют важную роль в сдерживании реакции неспецифического врожденного иммунитета на различные патогены. В частности, это в первую очередь относится к белку SOCS4 – супрессору сигнальных систем цитокинов 4. Будучи негативным регулятором контроля синтеза цитокинов, этот белок относится к ключевым факторам защиты от чрезмерной провоспалительной реакции на вирусную инфекцию. Белки-супрессоры этого семейства ингибируют сигнальный путь JAK/ STAT, тем самым контролируя звенья врожденного и адаптивного иммунного ответа [36].
SECISBP2 – ген, кодирующий ферментативный комплекс (Sec Insertion Sequence Binding Protein 2), который обеспечивает включение в структуру белков селеноцистеина [37]. Ферменты, содержащие селеноцистеин, входят в состав редокс-системы клеточной защиты от радикалов кислорода. Генерирование радикалов кислорода – это реакция клеток на большинство патогенных микроорганизмов, в том числе и вирусов [37]. При наличии наследственных мутаций в гене SECISBP2 усиление синтеза активных форм кислорода приводит к системному повышению чувствительности клеток к инсулину, что наблюдается, например, у мышей с нокаутированным геном, кодирующим селен-содержащий антиоксидантный фермент глутатионпероксидазу I. Клинически у человека носительство мутаций гена SECISBP2 проявляется азоспермией, аксиальной мышечной дистрофией, нарушением пролиферации Т-лимфоцитов и, в целом, иммуносупрессией. У носителей этих мутаций наблюдается высокий уровень перекисного окисления липидов и окислительного повреждения ДНК, снижение репаративного потенциала повреждений ДНК и укорочение теломер. Плейотропный эффект мутаций в гене SECISBP2 вызван нарушением функций всего селенопротеома [37]. Естественно, этот наследственный дефект особенно остро должен проявляться в случае заражения гриппом и развития гриппозной пневмонии. Известно, что антиоксидантная терапия гриппа позволяет достигать существенных терапевтических эффектов в отношении купирования интоксикационного синдрома и предупреждения сердечно-сосудистых осложнений [52].
ЗАКЛЮЧЕНИЕ
Понимание генетического полиморфизма в опреде-ленных генах позволяет ориентировать разработку системного лечения гриппа с акцентом на фенотипи-ческие проявления мутаций с учетом степени распро-страненности наследственной предрасположенности к тяжелым осложнениям гриппа среди групп генети-ческого риска и населения в целом.
Несмотря на возможность широкого распространения мутаций в пределах идентифицированных генов, ассоциированных с повышенной чувствительностью к гриппу, следует признать, что важнейшим фактором остается эффективность презентации вирусных антигенов в пределах популяционных групп с различными типами HLA [10, 12].
Смертность от гриппа регистрируется в острый пе-риод заболевания и обычно на пике эпидемии, а затем, как «отсроченная смертность», в период от 1-го до 3-х месяцев после перенесенного заболевания. Обычно ле-тальный исход связан с сопутствующими заболевания-ми, как правило, сердечно-сосудистой патологии. Чаще всего это инфаркт, нередко регистрируются инсульты. Таким образом, при анализе генетического фона попу-ляции необходимо учитывать и эти факторы.

